美国医药市场一直是全球市场的风向标,不仅是因为美国市场庞大,领导全球药品创新研发;还因为美国药品法规体系相对健全,在各个方面为各国药政机构提供参考和借鉴。1962年在美国诞生的cGMP,是世界上第一部GMP。其中,为了保护患者的安全,对于企业放行到市场上的药品,明确规定当发现缺陷时要及时召回。
在产品召回领域,美国是全球最早诞生产品召回制度的国家,从最早的1966年美国国会通过的《国家交通及机动车安全法》,制定并实施了一系列有关汽车产品安全召回的法规,后来召回制度又逐步扩大到了与人体安全健康有关的众多产品。美国对药品召回(Recall)的定义是企业对市场上销售的有缺陷产品的撤回(removal)或更正(correction),召回的类型主要有三种:企业自愿召回、FDA要求召回和强制召回。
《美国联邦法规》(英文简称是CFR)的第21章的7(C)部分为产品的自愿召回提供了一般性指导。另外,FDA在2003年11月3日发布的技术指南《产品召回指南(包括撤市和更正)》(Guidance for Industry: Product Recalls, Including Removals and Corrections)涵盖了更具体的建议,且适用于所有FDA监管产品的自愿和强制召回工作。
根据FDA官网公布的数据,据不完全统计,在2020年FDA共召回药品110例,医疗器械18例。今天,我们重点来汇总和分析一下2020年度的注射剂召回情况。
2020年FDA官网公布的注射剂召回事件共16起,均为自愿召回;导致这些召回发生的原因涉及交叉污染、产品混淆、防腐剂使用不当、发现微粒物质、高分子聚合物超标、杂质超标、空瓶或可能玻璃瓶破裂、贴错标签、安瓿瓶破裂、出现沉淀以及缺乏无菌保证导致所有无菌产品召回等(详见表1)。
表1- 2020年FDA的注射剂产品召回事件
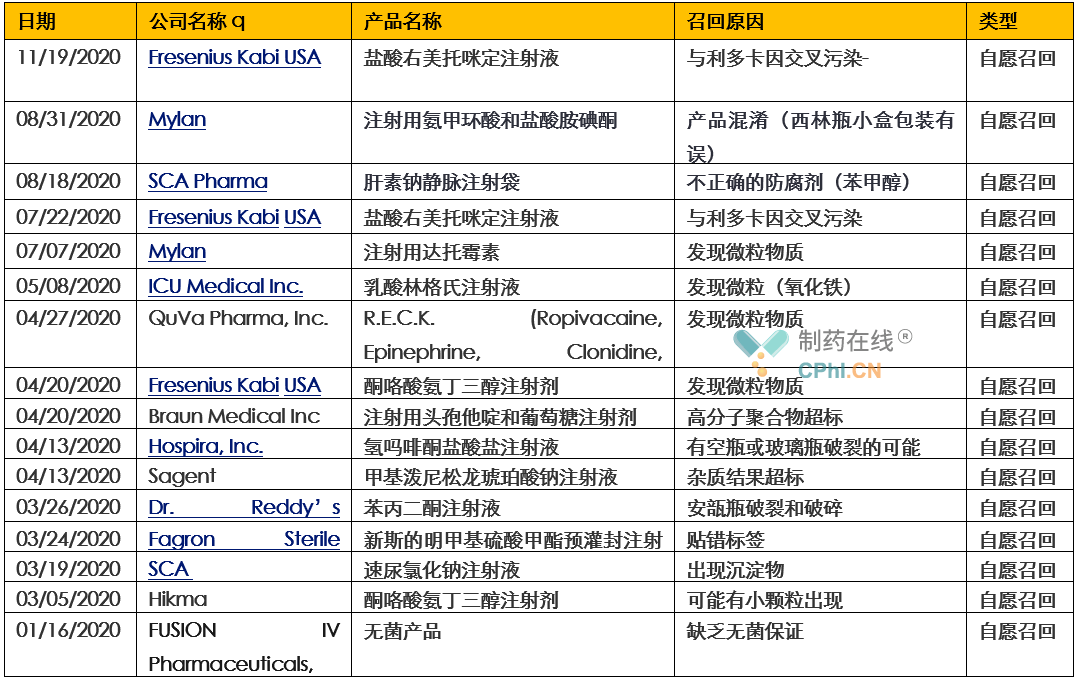
典型案例分析:
案例1-由于交叉污染导致的产品召回
2020年度费森尤斯卡比(Fresenius Kabi)共有3次召回,其中7月22日和11月19日的产品召回是由于同样的原因,均是注射剂产品( 盐酸右美托咪定)被另外一种活性成分(利多卡因)污染。这个公司在2019年底被中国药监局警告,并导致百济神州召回一款在中国市场销售的产品。
案例2-由于产品包装混淆导致的产品召回
2020年度迈兰制药(Mylan)共有2次召回,其中8月的召回原因是由于在小盒包装中存在注射用氨甲环酸和盐酸胺碘酮这两种注射剂的西林瓶发生了相互混淆。
另外一起类似的召回发生在3月24日,Fagron Sterile Services公司持有产品的召回是由于新斯的明甲基硫酸甲酯预灌封注射液的标签贴错。
案例3-由于发现微粒物质导致的召回
2020年度由于微粒物质导致的召回共5次,其中包括费森尤斯卡比(Fresenius Kabi)的酮咯酸氨丁三醇注射剂召回以及迈兰制药(Mylan)的注射用达托霉素召回等。如果静脉注射剂含有可见颗粒的溶液,可能会导致严重的不良事件,包括但不限于局部刺激、血管炎/静脉炎、抗原性或过敏性反应以及微血管阻塞,包括肺栓塞。这样严重的缺陷发生,说明生产这些药品的企业在硬件和软件方面都存在明显的缺陷;这样的缺陷也体现了质量体系的运行质量不佳。
案例4-由于防腐剂使用不当导致的召回
2020年8月SCA 制药的产品召回是由于其肝素钠产品中包含未声明的防腐剂苯甲醇。该产品标签上列出了防腐剂为对羟基苯甲酸甲酯和对羟基苯甲酸丙酯,不包含防腐剂苯甲醇。但是,现实情况是这些批次产品中存在的防腐剂苯甲醇与标签不一致。这个问题是SCA制药是在对产品低含量偏差调查的过程中发现的。对这个案例的分析,我们可以推测,这个偏差的发生,应该和不同种类产品之间的清洁操作不良有关。
案例5-由于结果超标导致的召回
2020年4月13日发生的Sagent Pharmaceuticals公司的甲基泼尼松龙琥珀酸钠注射液召回是由于杂质超标;另外4月20日Braun Medical Inc公司注射用头孢他啶和葡萄糖注射剂的召回是由于高分子聚合物超标。这个案例给制药行业从业者的警示信息是:这些产品很可能使用了不良的API,或者发生了不期望的原辅料不相容的事件。
案例6-由于缺乏无菌保证导致的所有产品的召回
2020年1月FUSION IV Pharmaceuticals, Inc dba. AXIA Pharmaceutcal公司发生的召回是由于该公司的无菌保证水平出现问题导致的大规模的无菌产品召回。这个案例所包含的产品很多,因此本文没有详细列入。但是从召回产品涵盖的品种和批次之多,可以推测:这个公司的质量控制体系基本失控,才会导致这样大面积的恶性事件发生。也说明,美国政府期望将部分产业引导回流到美国的愿望是多么难以实现。
案例7-某公司产品召回导致的其他公司产品召回的连锁召回
2020年4月QuVa Pharma, Inc.公司召回复合预灌封注射剂产品R.E.C.K. (Ropivacaine, Epinephrine, Clonidine, Ketorolac)是由于费森尤斯卡比(Fresenius Kabi)的酮咯酸氨丁三醇注射剂出现微粒物质召回引起的连锁反应。因为该产品为复合产品,其中的Ketorolac(酮咯酸氨丁三醇)是由费森尤斯卡比(Fresenius Kabi)制备的。这个案例比较有意思,可谓中国古语所云:城门失火,殃及池鱼。这个案例说明,在MAH选择受托生产企业时,要综合评估,避免选择了猪队友。
总结
从上面这些案例的具体信息和相关分析可以看出,美国制药行业的优势在商业运作和创新药研发。在传统药品制造领域,美国制药行业的优势也不是很明显。随着中国新修订《药品管理法》的实施,以及中国药品召回管理办法的修订,中国制药企业面临的合规压力也非常大。希望中国企业结合上面这些案例,充分评估自己的产品和管理的不足,持续提高质量与合规水平,确保运营安全。
说明:本文不构成任何投资判断和参考。
参考文献
1-FDA官网信息。
作者简介:zhulikou431,高级工程师、PDA会员、ISPE会员、ECA会员、PQRI会员、资深无菌GMP专家,在无菌工艺开发和验证、药品研发和注册、CTD文件撰写和审核、法规审计、国际认证、国际注册、质量体系建设与维护领域,以及无菌检验、环境监控等领域皆具有较深造诣。近几年开始着力关注制药宏观领域趋势分析和制药企业并购项目的风险管理工作。




合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57