4月7日,CDE官网显示,进口新药沙芬酰胺片正式向CDE提交上市申请,并获得受理。沙芬酰胺片去年让业内关注的原因就是正大天晴3类仿制药未获批。
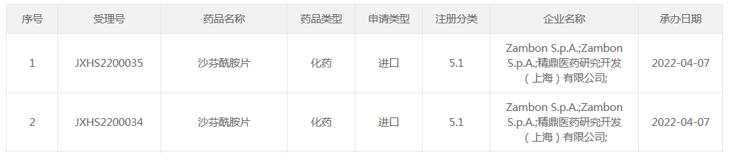
(资料来源:CDE官网)
近十多年以来最重要的帕金森药物
沙芬酰胺(又称沙非胺,Safinamide,商品名:Xadago/Equfina)是由Zambon和Newron共同研发的一款高度选择性、可逆的第三代单胺氧化酶B(MAO-B)抑制剂,能减少已分泌多巴胺的降解,帮助维持大脑中的多巴胺浓度,用于延长左旋多巴疗效。与雷沙吉兰、司来吉兰相比,具有两个优点:1、可以消除饮食的限制;2、具有抑制谷氨酸释放的附加功能,能对神经起到保护作用。
该药于2015年3月获得欧洲药监局批准上市,用于治疗中晚期帕金森病;于2017年3月获FDA批准上市,作为附加治疗药物,用于治疗正在服用左旋多巴/卡比多巴且出现“OFF”状态的帕金森患者,是美国近10多年来首 个获批用于治疗帕金森病的新化学实体,于2019年11月在日本获批;于2020年6月在韩国获批。
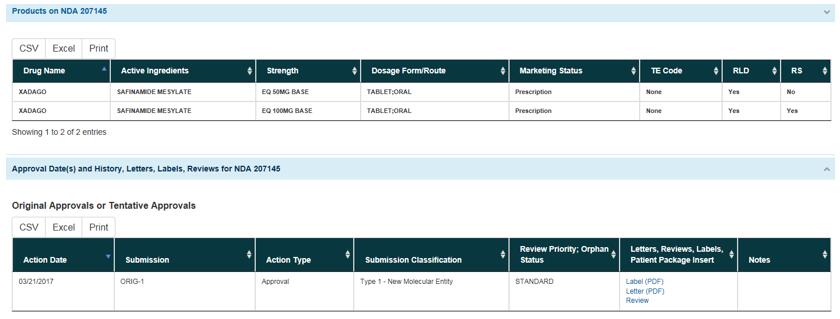
(资料来源:FDA官网)
据公开资料,甲磺酸沙非胺的化合物专利已到期。
正大天晴3类仿制药倒在黎明前
2020年12月,南京正大天晴提交3类仿制药甲磺酸沙非胺片的上市申请。
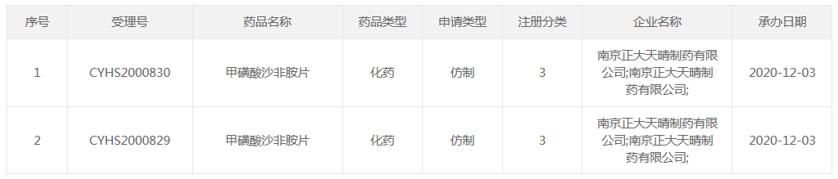
(资料来源:CDE官网)
2021年08月,NMPA官网发布药品通知件待领取信息,其中南京正大天晴的甲磺酸沙非胺片2个规格都未被批准,具体原因不得而知。
2020.12.03 药审中心承办
2020.12.04 审评任务启动
2021.06.03 完成药理毒理资料审评
2021.06.18 完成临床资料审评
2021.06.18 完成药学部分审评
2021.08.17 未被批准
审评时光轴可以看出,审评中未见发补情况,未见生产现场核查和临床试验现场核查等细节公布,最后直接审评结果为不批准。有业内人士推测,大概率还是临床数据问题。3类仿制药若只做BE试验就想通过审查,需要提供大量的临床数据证明可以在中国人群里具有安全性和有效性。
除此之外,扬子江和瑞阳制药正在进行BE试验,石药、永正药业和汉康医药甲磺酸沙非胺已经获批临床。
国内市场超过30亿元
根据中华医学会神经病学分会数据,国内帕金森病患者已超过300万人,65岁以上人群发病率为1.70%,每年新增患者将达10万左右。
MAO-B抑制剂是帕金森治疗药物中非常重要的一类,目前,该类药物在国际指南中已经成为早期PD单药治疗的一线选择。目前,国内批准两款MAO-B抑制剂,即司来吉兰、雷沙吉兰。
2020年第四版《中国帕金森病治疗指南》中,早期帕金森病强调了MAO BI(雷沙吉兰和司来吉兰)和DAs(罗匹尼罗)修饰疗法,并在MAO-BI中新增了沙芬酰胺、唑尼沙胺。
据米内网数据,在我国获批上市的帕金森治疗药物有15个化学名品种。2020年,国内重点省市公立医院帕金森治疗药物市场规模达6.3亿元,较上一年增长8.6%。位居前10位的是普拉克索片、多巴丝肼片/胶囊、恩他卡朋片、吡贝地尔片、司来吉兰片、雷沙吉兰片、苯海索片、恩卡他朋双多巴片、罗匹尼罗片和卡左双多巴片。
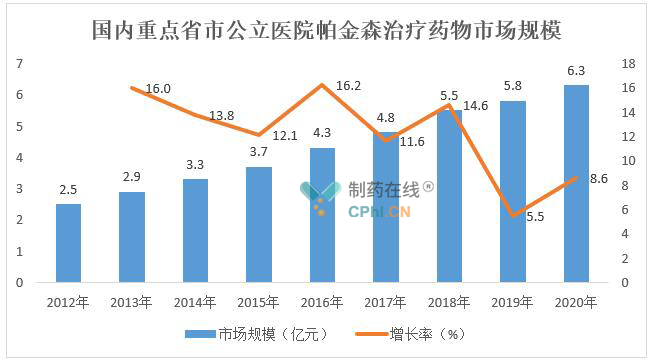
(根据公开资料进行整理)



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57