继化疗、靶向和免疫时代后,以细胞毒 性药物和靶向单抗偶联成药的ADC药物打开了肿瘤的第四阶梯药物治疗时代。ADC的设计理念由来已久,早在1906年,化疗之父、诺贝尔奖得主Paul Ehrlich教授首次提出"魔法子 弹"的概念,即将细胞毒 性药物安装在特异性单克隆抗体上,实现定向杀伤肿瘤细胞。
具体来说,抗体药物偶联物(ADC)由单克隆抗体 (mAb) 、linker、payload组成,自2000年,第一款ADC药物Mylotarg获FDA批准以来,目前全球共有15款ADC药物获批用于血液系统恶性肿瘤和实体瘤。
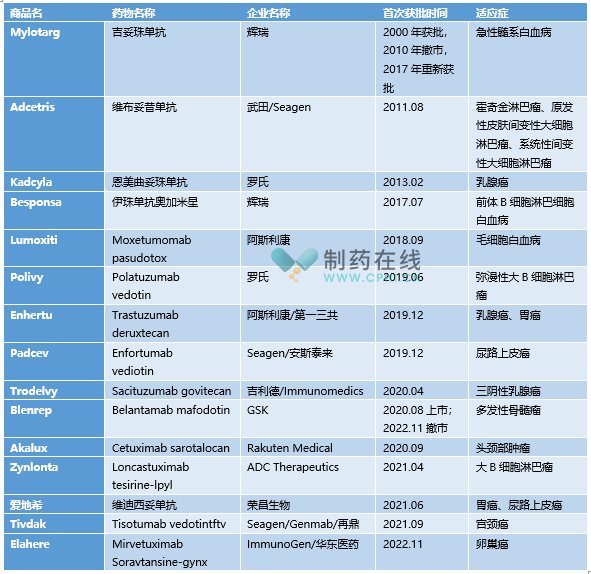
全球已获批上市ADC(公开资料、企业财报)
2022年,FDA仅批准了1款ADC药物,即Elahere(Mirvetuximab Soravtansine-gynx),由ImmunoGen公司研发,而ImmunoGen正是我们今天的主角。
深耕ADC赛道,向多家跨国药企做技术输出
ImmunoGen成立于1981年,属于国际上最早研发ADC药物的企业之一。1989年ImmunoGen在纳斯达克上市。ImmunoGen曾与Seagen、罗氏的Genentech一同并称为ADC领域的"三巨头"。ImmunoGen专有的喜树碱ADC药物开发平台旨在优化现有的喜树碱技术,以提供更宽的治疗窗,提高ADC药物的安全性和有效性。除此之外,它还构建了靶点筛选、抗体开发、毒素库、连接子库四位一体的ADC工具库。
2013年,ImmunoGen和罗氏共同研发的HER2 ADC药物Kadcyla获FDA批准,用于HER2+转移性乳腺癌患者的治疗。2020年,Kadcyla获NMPA批准上市,成为国内第一款上市的ADC,也是目前商业化最成功的ADC之一
除Kadcyla外,ImmunoGen还开发了Elahere,这是全球首 款靶向叶酸受体α(FRα)的ADC药物,由FRα结合抗体、可裂解的连接子和美登木素生物碱DM4组成。Elahere将与FRα结合的人源化单克隆抗体,与能够产生细胞毒 性的DM4分子通过二硫键连接起来。当ADC与FRα结合之后,FRα能够将ADC转移到细胞内部,ADC携带的细胞毒 性分子从而抑制肿瘤细胞的有丝分裂。Elahere于2022年11月获得FDA批准加速上市。
今年5月3日,ImmunoGen宣布Elahere的III期验证临床MIRASOL试验获得成功,成为首 个延长铂耐药卵巢癌患者总生存期(OS)的新药。研究结果表明,Elahere治疗组相比于化疗组,OS从12.75个月延长到16.46个月,死亡风险降低33%。无进展生存期(PFS)从3.98个月延长到5.62个月,疾病进展或死亡风险降低35%。客观缓解率(ORR)从15.9%提高到42.3%,且安全性优于化疗。
Elahere的成功打开了ADC治疗卵巢癌的想象空间,ImmunoGen股价受此影响,当天大涨136%。
基于强大的ADC技术平台,技术授权许可是ImmunoGen的主要收入来源。目前,ImmunoGen与安进、拜耳、罗氏、礼来等公司均有技术授权合作。
|
交易时间 |
受让方 |
交易药品 |
交易类型 |
|
2004.10 |
Biogen |
|
合作/许可 |
|
2004.12 |
Janssen Biotech |
IMGN388 |
许可 |
|
2005.07 |
Genentech |
— |
许可 |
|
2005.12 |
Genentech |
— |
许可 |
|
2006.07 |
Biotest |
Indatuximab ravtansine |
许可 |
|
2006.10 |
Sanofi |
— |
许可 |
|
2006.12 |
Sanofi |
— |
合作/期权 |
|
2008.01 |
Bayer |
Anetumab ravtansine |
合作/许可 |
|
2008.08 |
Sanofi |
— |
许可 |
|
2008.12 |
Genentech |
— |
许可 |
|
2009.09 |
Amgen |
AMG172 |
许可 |
|
2009.11 |
Amgen |
AMG595 |
许可 |
|
2010.10 |
Novartis |
HKT288,PCA062, LOP628 |
合作/许可 |
|
2011.12 |
礼来 |
LY3076226 |
合作/许可 |
|
2012.12 |
Amgen |
— |
许可 |
|
2013.11 |
Novartis |
— |
许可 |
|
2013.12 |
Sanofi |
SAR428926 |
许可 |
|
2014.05 |
Oxford BioTherapeutics |
— |
许可 |
|
2015.03 |
Takeda Pharmaceuticals |
TAK-164 |
许可/期权 |
|
2017.05 |
Debiopharm |
Naratuximab emtansine |
收购 |
|
2017.05 |
Sanofi |
Isatuximab,tusamitarnab |
许可 |
|
2017.08 |
Jazz Pharmaceuticals |
IMGN779, pivekimab sunirine |
期权/合作 |
|
2020.10 |
华东医药 |
Mirvetuximab soravtansine |
合作/许可 |
|
2020.11 |
Viridian Therapeutics |
AVE1642 |
许可 |
|
2022.02 |
礼来 |
— |
许可/合作 |
|
2022.12 |
博奥信生物 |
— |
合作 |
|
2023.03 |
Vertex Pharmaceuticals |
— |
期权 |
ImmunoGen对外授权项目(公司公告)
ImmunoGen其他ADC管线梳理
►IMGC936
IMGC936是由高亲和力的人源化单克隆抗体、美登木素生物碱微管抑制剂载荷和稳定的三肽接头偶联而成,DAR为2,提高了肿瘤渗透率和药物递送率。IMGC936由ImmunoGen与Macrogenics合作开发,靶向ADAM9。
ADAM9是一种细胞表面蛋白,属于蛋白酶ADAM家族,与细胞因子和生长因子的脱落以及细胞迁移有关。ADAM9的失调与肿瘤的进展和转移以及病理性新血管形成有关。由于ADAM9在多种实体瘤中过表达,但在正常组织的表达量较少,因此,ADAM9成为ADC研发的一个有吸引力的靶点。
IMGC936正在进行I期临床研究,主要针对包括NSCLC、TNBC、CRC等在内的晚期实体瘤。
►IMGN632
IMGN632是一种靶向CD123的ADC,由ImmunoGen研发。CD123是异二聚体白细胞介素-3受体(IL-3R)的亚基, IL-3R是β共同受体家族成员。这种膜受体家族在调节造血细胞的生长、增殖等过程中发挥着重要作用。CD123在各种血液系统恶性肿瘤中广泛表达,但在正常细胞中低表达,这使CD123成为非常有吸引力的靶点。
IMGN632,采用了ImmunoGen新型的吲哚-苯并二氮杂(IGN)载荷(payloads)。这种载荷可以在不发生交联的前提下,将DNA烷基化,导致单链DNA损伤。目前,IMGN632正在进行两项临床研究,分别针对母细胞性浆样树突细胞肿瘤(BPDCN)和急性髓性白血病(AML)。
ImmunoGen成立四十余年来,一直致力于ADC药物的研发。当前在创新药领域,条条赛道慢慢变得拥挤,而最终只有像ImmunoGen一样,拥有自己的核心技术,才能避免同质化竞争,开发出切实满足患者临床需求的产品。
主要参考资料:
[1]https://investor.immunogen.com/static-files/c13665c0-ef8c-4529-9f67-faa0ff4db62a;
[2] https://www.nature.com/articles/s41392-022-00947-7;
[3] https://investor.immunogen.com/news-releases/news-release-details/immunogen-announces-fda-breakthrough-therapy-designation-imgn632.



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57