美国当地时间1月25日,FDA发布公告召回一款硫酸右旋苯 丙胺片,原因是贴错标签。

图源FDA
据悉该药物已经到了医疗机构,是被一名药剂师发现了问题。药剂师在开瓶时发现硫酸右旋苯 丙胺片的瓶子里装的是马来酸卡比沙明。不清楚是否在相关产品的说明书或者标签中明确了药物的外观形态,也可能是药剂师有过同类药物的使用经验。所以直接将一侧印有"GL",另侧印有"211"的白色圆形片剂识别出。而正常的药物应为浅黄色六边形,一侧印着"30",一侧印着"MIA"。其中"30"代表其规格30毫克。

图源FDA
尚不清楚这两种药的瓶子是否为同一类型,如果是同一类型的内包装瓶,那可能是贴错标签。如此一来,可能存在大面积的混淆。因为就压片数量而言,会有物料平衡,一批货中间品能出多少片,就对应着成品的瓶数。两种药,这个成品多了,那个成品必然少了。出现这种情况时,容易被察觉。但如果是互相混淆,那可能就从两个批次的成品数量上看不出来。再说了,怎么能把两种内包装一样的无标识药品放在同一空间呢?难道你们是把装瓶拧盖、贴标签分在两个流程,没有连起来吗?
如果根本就不是同一类型的瓶子,那可能不是简单的贴错标签就能解释得通。往往预示着装瓶时前期的清场不彻底,换句话说,先产的误入的药,然后有剩余未做清场,就直接装后面的药,混了。因为前面的药剩余量不大,所以未能引起大量的成品量波动。最终没能发现问题。
但其实这里都有几个问题,一是清场不彻底;二是物料平衡走过场。如果是本身两种药片的重量不一样,那还有一个问题就是没有在线称重来确定装量差异。通俗点讲,甲药片每粒0.3克,乙药品每粒0.45克,那30片就有30*0.15=4.5克的差异。如果瓶子本身重量很接近,那就可以从在线称重时发现问题。然而多个把控程序并没有发现问题,只能说流程控制做的太粗糙了。
还有一点,这样的明显药片外观不同,形状、颜色、标识完全不同,理论上是利于生产员工发现问题的。但这种发现更多的是依赖目测,也就是说工人在分装时要能一直看到待分装药品。在现在自动化程度如此之高的情况下,靠人工发现问题,已经变得很不现实了。所以外观性状的差异,反而是到了使用环节才被发现。
就涉事的产品种类硫酸右旋苯 丙胺而言,国内只有华润双鹤药业有类似产品。
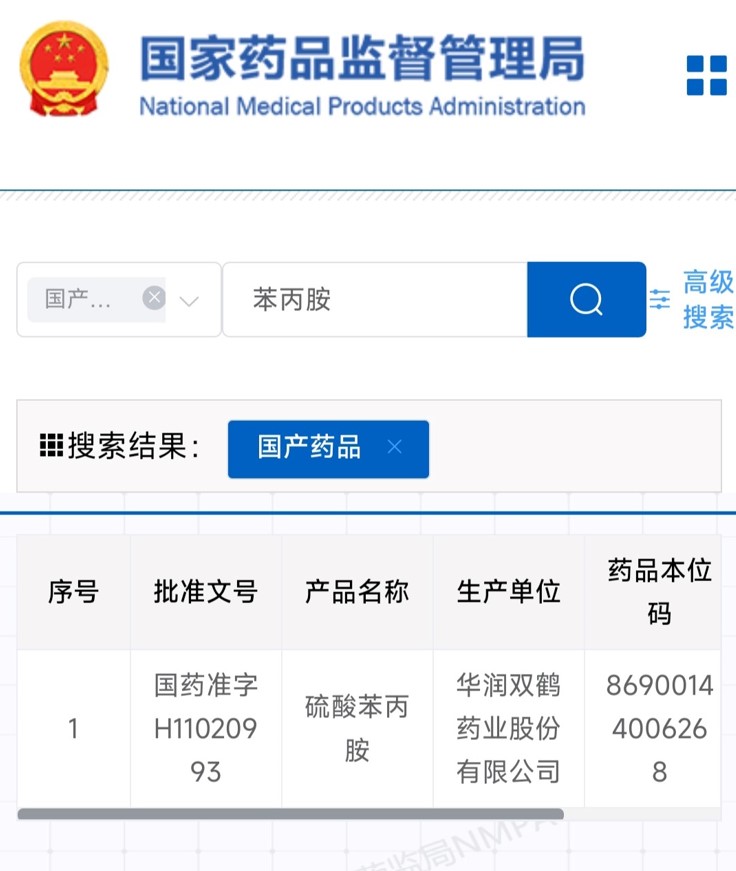
图源药监局
而误入的马来酸卡比沙明则没有同类药品上市,但有相关资料显示该复合品种药物因含有苯丙醇胺被禁止销售和使用。
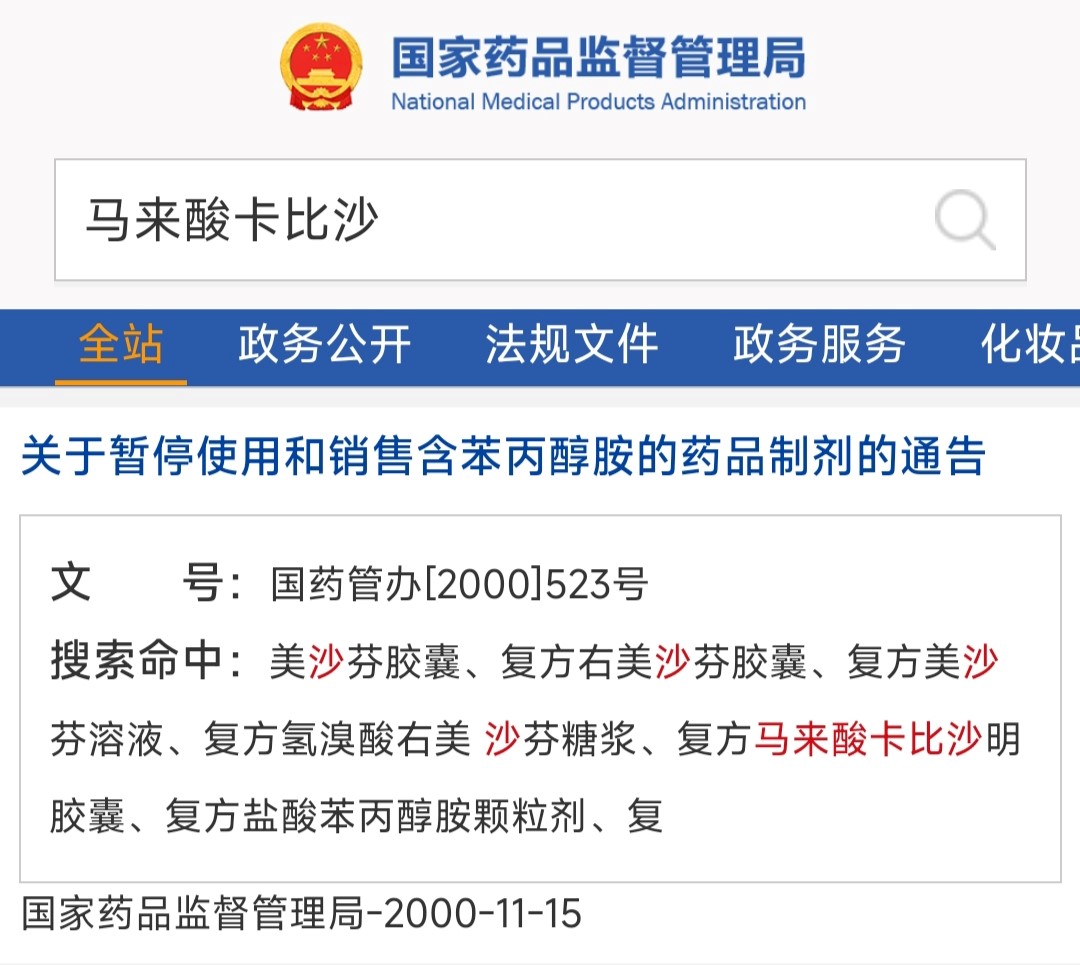
图源药监局
两种药物的治疗领域差异之大,也是容易引发问题的原因之一。硫酸苯 丙胺属于中枢兴奋药,而马来酸卡比沙明则是用来抗过敏的,可能会导致嗜睡。进而引发一系列的社会问题,比如驾驶车辆、操作大型设备时睡着。类似的事件曾在日本发生过,当时是抗真菌药错误投料安 眠药,导致用药人驾车交通事故出现人身伤亡。所以很多药物的误用,并非简单的医疗问题,可能会引发更多的社会问题。
我们很难通过某个单一操作就能杜绝风险,所以物料平衡和清场这些简单的死规定,才显得尤为重要。在美国的体系下,如果出现继发的药物不良事件,尤其是上升到社会事件后,恐怕不是一个鞠躬就可以解决的了。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57