
丁二酸复瑞替尼胶囊(SAF-189s)是复星医药研发的新一代高效、具有中枢神经系统(CNS)渗透性的ALK/ROS1抑制剂,于2025年3月6日获得中国国家药监局药品审评中心(CDE)的上市申请受理。
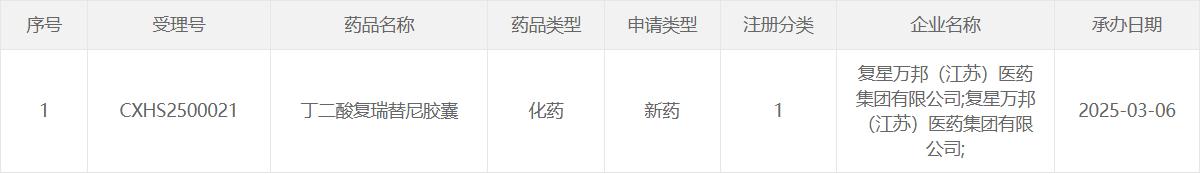
图源:CDE官网
丁二酸复瑞替尼胶囊是一种小分子化学药物,靶向ALK(间变性淋巴瘤激酶)和ROS1(ROS原癌基因1)两个重要的肿瘤驱动基因,复瑞替尼通过抑制ALK和ROS1激酶的活性,阻断肿瘤细胞的增殖和生长信号通路,从而发挥抗肿瘤作用;复瑞替尼具有显著的血脑屏障透过能力,能够有效抑制中枢神经系统(CNS)的肿瘤进展,这一特性使其在治疗脑转移患者时具有显著优势,尤其是在ALK阳性NSCLC患者中,脑转移的发生率较高,传统药物往往难以有效控制。
一、需求驱动下的复瑞替尼前期探索
丁二酸复瑞替尼胶囊的研发背景源于对非小细胞肺癌(NSCLC)治疗领域未满足临床需求的深刻洞察。NSCLC是肺癌中最常见的类型,占所有肺癌病例的80%-85%,其中约5.6%的患者存在间变性淋巴瘤激酶(ALK)基因突变;ALK基因重排是非小细胞肺癌的重要治疗靶点之一,其融合蛋白在肿瘤细胞的增殖和转移中起关键作用。近年来,ALK抑制剂已成为治疗ALK阳性NSCLC的重要手段,但现有药物在耐药性和中枢神经系统(CNS)渗透性方面仍存在不足;许多患者在治疗过程中会出现耐药,导致疾病进展,尤其是脑转移的发生率较高,这使得开发新一代ALK抑制剂成为当前研究的热点和难点。在此背景下,复星医药与控股子公司重庆复创医药研究有限公司(复创医药)共同启动了丁二酸复瑞替尼胶囊的研发项目。
丁二酸复瑞替尼胶囊的研发始于临床前研究阶段。研究人员通过大量的合成与筛选工作,成功合成了具有高效ALK/ROS1抑制活性的小分子化合物SAF-189s。临床前研究显示,该化合物不仅具有强大的体外抗肿瘤活性,还在裸鼠移植瘤模型中展现出良好的体内抗肿瘤效果,还具有良好的药代动力学特征和安全性,这些结果为其后续的临床试验奠定了坚实的基础。
2015年1月30日,重庆复创医药研究有限公司与中国科学院上海药物研究所共同向国家食品药品监督管理总局提交了丁二酸复瑞替尼胶囊的临床试验申请,并获得受理;在审批过程中,该药物获得了特殊审评程序及重大专项优先审评资格;同年10月29日,该药物的临床试验申请正式获批,标志着其研发进入临床试验阶段。
二、临床试验的亮眼表现
在临床试验阶段,丁二酸复瑞替尼胶囊的研发稳步推进。Ⅰ/Ⅱ期临床试验在中国境内多家研究中心进行,并在2022年ASCO大会上,丁二酸复瑞替尼胶囊的1/2期试验结果公布,I 期试验里,未接受过 ALK 抑制剂治疗和接受过预处理的两类患者 DCR 均为 100%;II 期试验中,未接受过治疗患者 ORR 为 92.3%、DCR 为 98.1%,接受过克唑替尼治疗患者 ORR 为 65.4%、DCR 为 88.5% 。
基于Ⅰ/Ⅱ期临床试验的积极结果,复星医药启动了丁二酸复瑞替尼胶囊的Ⅲ期临床试验。试验评估了药物患者中的疗效和安全性,为上市申请提供临床数据支持。2024年世界肺癌大会(WCLC)期间,公布了丁二酸复瑞替尼胶囊的Ⅲ期REMARK研究中期结果,针对未经治疗的ALK阳性晚期非小细胞肺癌患者,复瑞替尼组(160mg每日一次)与克唑替尼组(250mg每日两次)相比,无进展生存期(PFS)显著延长,中位PFS未达到(对照组13.93个月),风险比(HR)为0.23。对于基线脑转移患者,复瑞替尼的颅内客观缓解率(ORR)达100%,显著高于对照组的50%,且中枢神经系统进展风险降低96%(HR 0.04)。总体ORR为92.8%,较对照组提升12%(P=0.0035)。安全性方面,3/4级治疗相关不良事件发生率为37.7%,低于对照组的55.6%,未报告致死性事件或间质性肺病。
总结
经过多年的努力,丁二酸复瑞替尼胶囊的研发取得了重要进展。2025年3月6日,新药丁二酸复瑞替尼胶囊的上市申请获得受理,标志着该药物距离上市又迈出了重要一步。
丁二酸复瑞替尼胶囊也展现出广阔的应用前景,尽管全球已有克唑替尼、阿来替尼等ALK抑制剂上市,但现有疗法仍面临一些挑战,例如ALK阳性NSCLC患者会出现脑转移,而传统药物因血脑屏障穿透力不足导致颅内病灶控制率偏低以及安全性问题等;但复瑞替尼的临床数据则展现出破局之势,为患者提供了全新解决方案。
参考资料:
[1]Yang J J, Zhou J, Cheng Y, et al. SAF-189s in advanced, ALK-positive, non–small cell lung cancer: Results from a first-in-human phase 1/2, multicenter study[J]. 2022.
[2]Xiong A, Yang N, Dong X, et al. OA09. 03 Randomized, Open-Label, Phase III Study of SAF-189s Versus Crizotinib in First-Line ALK-Positive Advanced Non-Small Cell Lung Cancer (NSCLC)[J]. Journal of Thoracic Oncology, 2024, 19(10): S27-S28.



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57