近日,双鹭CTLA-4单抗MV049进入Ⅰ期临床,成为继信达的IBI310(单抗)和康宁杰瑞的KN044(单域抗体Fc融合蛋白)后,第三个进入临床的CTLA-4单抗。
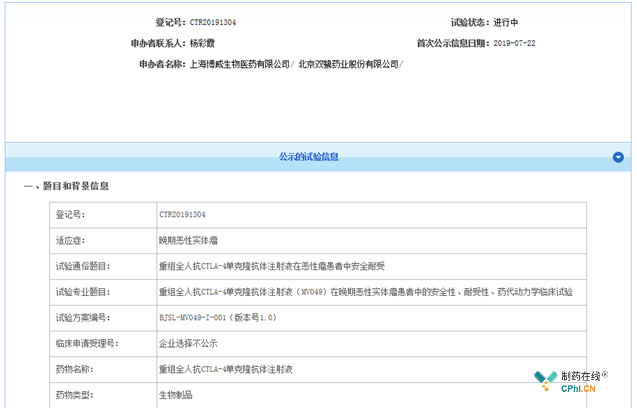
(资料来源:"药物临床试验登记与信息公示平台")
CLTA-4单抗:与PD-(L)1单抗联用威力大
作用机制:
CTLA-4分子(细胞**T淋巴细胞相关蛋白4)高表达于调节性T淋巴细胞(Treg)和激活的T淋巴细胞上,与CD28共同享有抗原呈递细胞(APC)的B7分子配体,CTLA-4与B7分子结合后诱导T细胞无反应性,参与免疫反应的负调节。CTLA-4在多种癌症中过表达,导致肿瘤生长失控。而CTLA-4抑制剂可阻断CTLA-4通路的激活,增强T细胞活化及增殖,下调T-reg介导的免疫抑制。
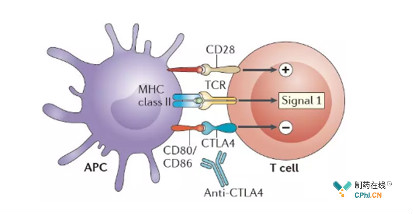
CTLA-4抑制剂作用机制
代表药物:
伊匹单抗(Ipilimumab,商品名:Yervoy),由BMS研发,是FDA批准的首个也是唯一一个CTLA-4 抑制剂,获批适应症为黑色素瘤(2011)、肾癌(2018)以及结直肠癌(2018)。
由于伊匹单抗可能出现致命的不良反应和异常严重的副作用,药物标签带有严重风险的黑框警告,因此全球销售额在过去8年间未超过15亿美元,与作用机理类似的PD-(L)1单抗纳武单抗(Nivolumab,商品名:Opdivo)的67.35亿美元相差甚远。
伊匹单抗2011-2018全球销售额(亿美元)
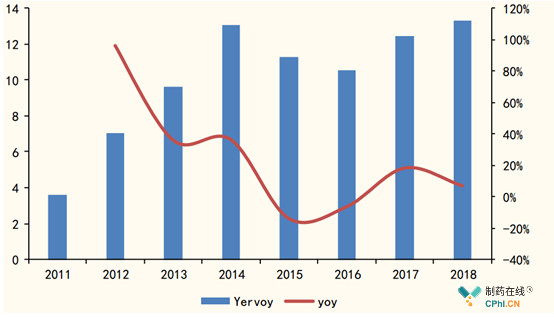
(数据来源:公司年报)
与PD-(L)1单抗联用:
伊匹单抗单独用药,病人存在较大比例不应答,出现3-5级不良事件的概率为13.3%,这限制了单药的应用前景。因此,CLTA-4单抗与其他免疫抑制剂联用成为趋势,特别是CTLA-4单抗和PD-(L)1单抗联用在临床上被证明具优效的免疫治疗策略,可以提高PD-(L)1单抗在转移性结直肠癌(mCRC)、黑色素瘤、肾癌以及非小细胞肺癌(NSCLC)的商业价值。
转移性结直肠癌(mCRC)
2018年7月,FDA加速批准伊匹单抗与纳武单抗联合用于治疗12岁及以上患有微卫星高度不稳定性(MSI-H)或错配修复缺陷(dMMR)转移性结直肠癌(mCRC)且使用氟嘧啶、奥沙利铂和伊立替康治疗后进展的患者。
黑色素瘤
随着Keytruda(派姆单抗)和Epacadostat(IDO 抑制剂)在III期试验的失败,目前PD-1单抗和CTLA-4 单抗联用对黑色素瘤疗效。
各一线治疗黑色素瘤的试验结果对比
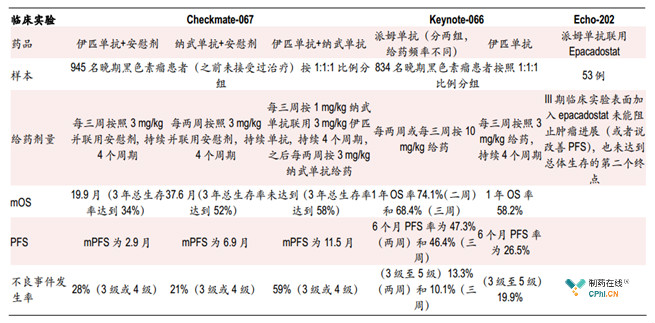
(资料来源: New England Journal of Medicine)
肾癌
纳武单抗联合伊匹单抗针对晚期肾癌的 III 期临床试验(Checkmate214)数据表明,相比于舒尼替尼,纳武单抗和伊匹单抗联用可大幅延长晚期透明细胞肾癌患者生存期。
纳武单抗与伊匹单抗联合治疗晚期肾癌的III期临床试验
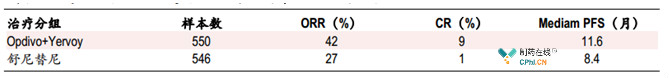
(资料来源:ASCO)
2018 年4月,AACR年会上宣布了一项III期临床(Checkmate-227)的初步研究结果,该研究评估了重磅免疫疗法纳武单抗加低剂量伊匹单抗一线治疗III期/IV型非小细胞肺癌(NSCLC)患者的效果。CheckMate-227结果显示,无论PD-L1表达水平,在鳞状和非鳞状肿瘤组织学中纳武单抗联合伊匹单抗治疗高肿瘤突变负荷患者(TMB)的无进展生存期(PFS)明显长于化疗。 Opdivo+Yervoy 联合治疗1年无进展生存率为42.6%,中位无进展生存期为 7.2 个月;化疗的 1年无进展生存率为 13.2%,中位无进展生存期为5.5个月。 Opdivo+Yervoy 的客观缓解率为 45.3%,化疗的客观缓解率为 26.9%。Opdivo+Yervoy 治疗 3 或 4 级治疗相关不良事件的发生率为 31.2%,化疗的同类发生率为 36.1%。
Opdivo+Yervoy 联合一线治疗 III 期/IV 型非小细胞肺癌(NSCLC)患者的疗效
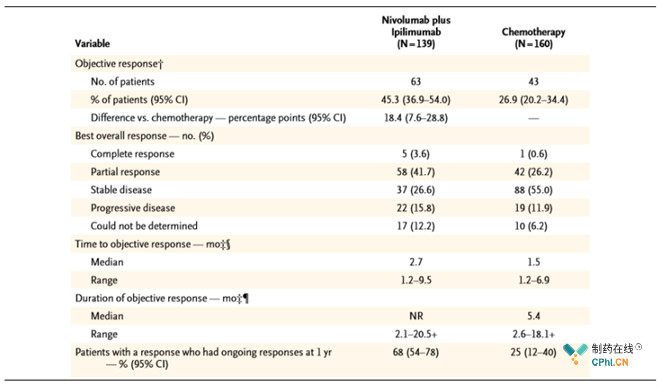
(资料来源:《NEJM》)
10家中国企业布局,信达、康宁杰瑞、双鹭进度最快
目前,有10中国家企业已布局 CTLA-4 靶点药物,共 11 个品种,均处于临床早期或临床前阶段。从药品类型看,单抗、双抗、单域抗体和CAR-T细胞疗法均有涉及,其中信达生物进度较为靠前。
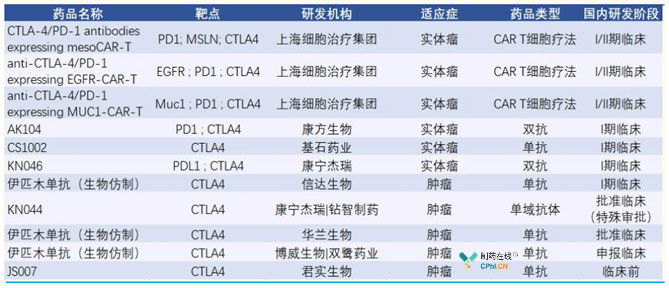
(资料来源:医药魔方)
笔者查询"药物临床试验登记与信息公示平台",目前国内开展的CTLA-4抑制剂临床试验如下:

可以看出,康宁杰瑞的KN044、KN046以及KN019均属于CTLA-4抑制剂(可能是一个品种,只是代号发生改变),开展了类风湿性关节炎的临床试验。而康方生物的AK104也紧随双鹭之后开展了临床试验。
作者简介:菜菜,上海交通大学药学硕士,曾工作于科学技术情报研究所,现为药监系统从业人员,擅长解读行业法规、最新药研动态等。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57