近日,东阳光药提交了旗下在研1类新药磷酸依米他韦胶囊的国内上市申请,该疗法有望成为国产首批全口服抗丙肝新药。
1.1类丙肝口服直接抗病毒 药物
近年来,直接抗病毒 药物(Direct acting agents,DAA)进展迅速,鉴于该类药物可口服、获得持续病毒学应答率(SVR)高、疗程短等诸多优势,丙肝患者的治疗方式已经发生了很大的改观。
磷酸依米他韦是东阳光自主研究开发的一种丙肝病毒NS5A蛋白抑制剂,拟与其他药物联合用于肝功能代偿慢性丙型肝炎的抗病素治疗。
2014年1月,东阳光药向CFDA提交了磷酸依米他韦的临床试验申请,2014年11月获得Ⅰ期临床试验批件,2016年12月获得了Ⅱ/Ⅲ临床试验批件。
基于Ⅲ期临床试验(登记号:CTR20180228)的结果,东阳光药近日递交了磷酸依米他韦的国内上市申请,该新药是东阳光药首个递交上市申请的国家1.1类新药,同时也将有望成为在中国国内实现商业化的首批国产自主研发的DAA药物。
两种临床治疗方案
在临床治疗方面,东阳光药围绕磷酸依米他韦主要推进了丙肝的两种治疗方案。
方案一的Ⅲ期临床试验在国内招募360名患者,通过磷酸依米他韦与索磷布韦联用,以治疗结束后12 周时实现持续病毒应答的受试者百分比(SVR12)为衡量指标,评价磷酸依米他韦联用索磷布韦治疗基因1型慢性丙肝患者的抗病毒疗效、安全性和耐受性。目前,该项临床试验已完成。
另外一种治疗方案始于东阳光与太景医药的合作。2016年,双方达成合作协议,设立合营公司,将磷酸依米他韦与伏拉瑞韦合并以开发新型丙型肝炎全口服免干扰素合并疗法。伏拉瑞韦是由太景医药开发的丙肝NS3/4A蛋白酶抑制剂,按照协议,东阳光药磷酸依米他韦开发成功之后,太景医药将获该药有关研究、开发、生产及销售的全球独占许可。
目前,磷酸依米他韦与伏拉瑞韦联用的II期临床试验已经完成。在依米他韦与伏拉瑞韦联合使用的Ⅱ期临床试验中,治疗结束后12周时,患者血清的SVR12高达97.4%,有效性及安全性良好。目前已经启动了Ⅲ期临床试验,拟在国内招募360名受试者,以治疗结束后12周时实现持续病毒应答的受试者所占比例为衡量指标,评价伏拉瑞韦胶囊、磷酸依米他韦胶囊与利巴韦林联合给药12周治疗感染慢性丙型肝炎病毒基因1型的抗病毒疗效。
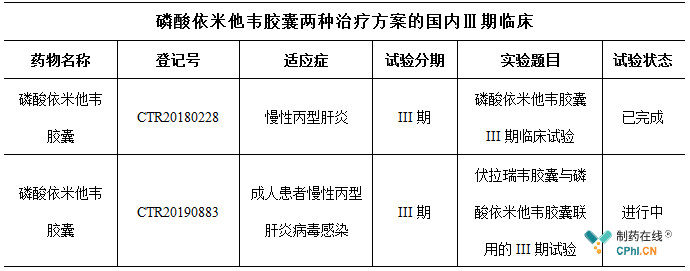
数据来源:药物临床试验登记与信息公示平台
首批国产二联DAA潜力治疗药物
2018年,东阳光药营业额为25.1亿元,较去年同期增长56.8%。其中,可威颗粒剂、可威胶囊剂、尔同舒的销售额增长率分别为68%、43%及149%,构成了东阳光药2018年度业绩增长的主要动力。
在丙肝治疗领域,依米他韦/索磷布韦、依米他韦/伏拉瑞韦的组合定位为将在中国实现商业化的首批国产二联DAA治疗药物,两种药物组合均为全口服治疗方案,这将大大提高患者的治疗依从性。
基于目前的临床试验结果,磷酸依米他韦两种治疗方案的疗效及安全性良好,与索磷布韦联用的上市申请已提交,若未来顺利通过审评审批上市,那么该丙肝疗法有望成为东阳光药在丙肝治疗领域的主打产品之一,进一步丰富公司的产品线。
作者简介:小药丸,制药行业从业者,自媒体时代的文字搬运工,专注于制药圈内的阴晴冷暖。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57