近日,荣昌生物自主研发的泰它西普亮相第四届中国医药创新与投资大会,用于系统性红斑狼疮治疗的临床数据进行了全球首发展示,受到了业界的普遍关注。
系统性红斑狼疮治疗领域 国产First-in-Class创新药物
系统性红斑狼疮(SLE)是一种慢性、多系统受累的自身免疫性疾病,以B淋巴细胞异常激活并异常分化为浆细胞和记忆性效应细胞,产生大量的自身抗体为特征,严重威胁了人类健康。很久以来,临床缺乏针对SLE特异性的治疗药物,对于SLE的常规治疗主要还是糖皮质激素和免疫抑制剂为主,皮质激素是全部治疗方案的基础,环磷酰胺是治疗重症狼疮性肾炎的重要药物,但不良反应较大限制了其临床使用。
2011年3月,GSK旗下创新药贝利木单抗经FDA批准上市,用于系统性红斑狼疮的治疗,2018年的全球销售额为4.73亿英镑。
作为一种完全人源化IgGI-X单克隆抗体,贝利木单抗能够选择性结合B-淋巴细胞刺激因子(BLyS)蛋白,阻断BLyS引起的B细胞自我破坏,降低不良反应的发生,对机体正常的免疫功能无明显损害,较传统治疗药物具有明显优势,开启了全球为系统性红斑狼疮的生物靶向治疗时代。2019年7月,贝利木单抗在我国的进口上市申请(JXSS180005/6)获得批准,中国市场即将成为这款新药未来业绩增长的新动力。
泰它西普是荣昌生物自主研发的具有全新结构与作用靶点的生物新药,属于重组人 B 淋巴细胞刺激因子受体-抗体融合蛋白,能同时靶向抑制BLyS和APRIL两个细胞因子,拟用于系统性红斑狼疮、类风湿性关节炎等多种自身免疫疾病的治疗,有望成为系统性红斑狼疮治疗领域First-in-Class的国产新药品种。
临床试验
截至目前,荣昌生物围绕泰它西普在国内已开展了多项临床试验,适应症覆盖了系统性红斑狼疮、原发性干燥综合征、视神经脊髓炎谱系疾病及类风湿性关节炎等疾病,其中用于系统性红斑狼疮、类风湿性关节炎的部分Ⅱ期临床上试验已完成。
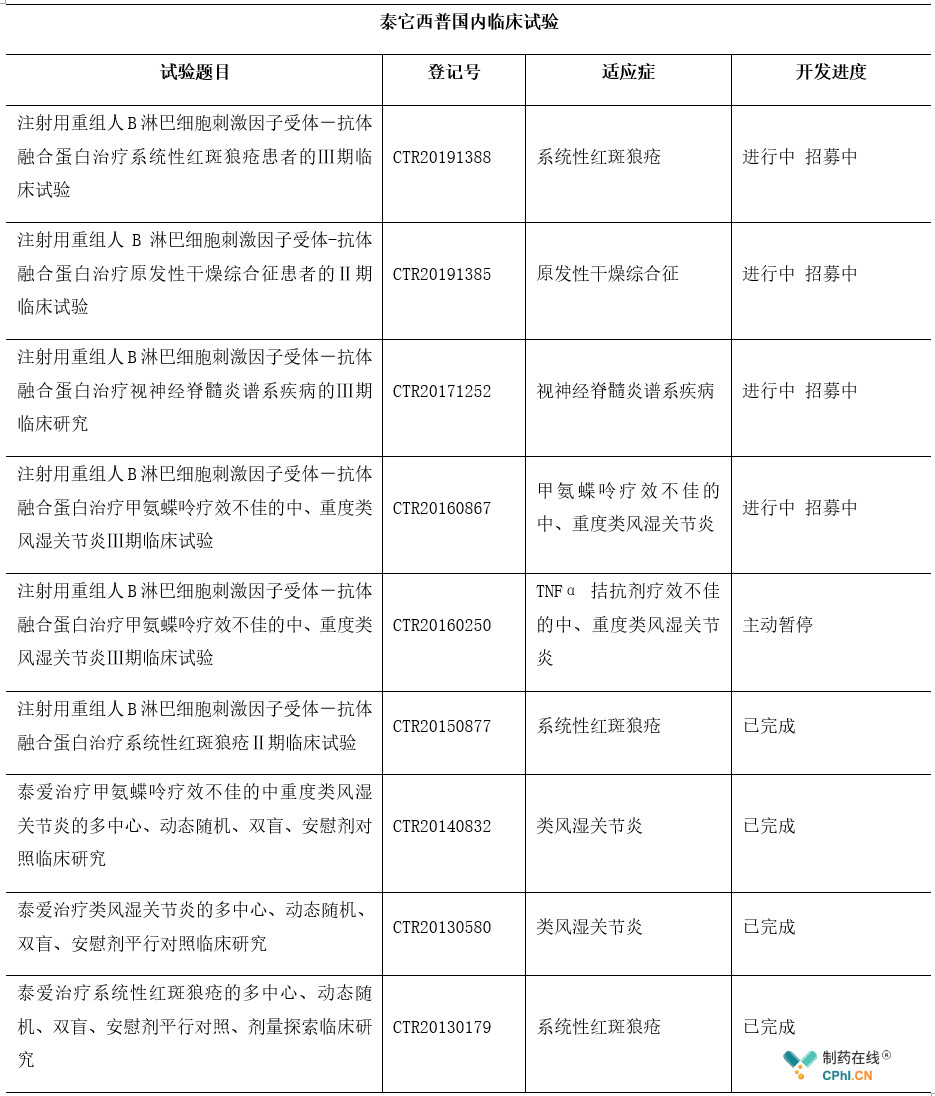
数据来源:药物临床试验登记与信息公示平台
2016年,泰它西普用于系统性红斑狼疮的关键性临床试验(CTR20150877)启动,这项多中心、随机、双盲、安慰剂对照的Ⅱ期临床研究旨在初步评价泰爱联合标准疗法与安慰剂联合标准疗法治疗中重度SLE患者的安全性和有效性,并分析其量效关系,为后续临床试验提供剂量依据。首例受试者于2016年3月入组,实际入组人数249人,主要终点指标为用药12个月SLE应答指数,该项试验已经于2019年6月完成。
从目前公布的试验结果来看,试验达到了主要的临床终点,次要终点结果与有效性结果相符,受试人群耐受性良好。
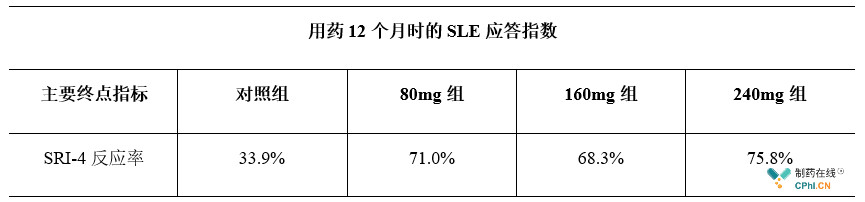
资料来源:公开资料整理
在海外临床试验方面,目前泰它西普已获得了FDA准予Ⅱ期临床试验(IND)的许可,用于系统性红斑狼疮的全球多中心临床试验即将启动,这是泰它西普这款国产创新药迈向欧美等海外市场上市征程的重要一步。
专利布局
在专利布局方面,荣昌生物围绕泰它西普在国内申请了制备方法、用途专利,均已获得授权。
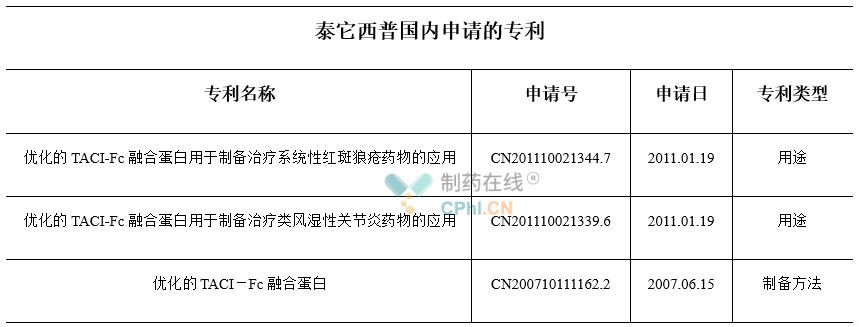
数据来源:NIPA
作者简介:小药丸,制药行业从业者,自媒体时代的文字搬运工,专注于制药圈内的阴晴冷暖。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57