12月12日,CDE网站更新消息,和黄医药1类新药索凡替尼的上市申请被拟纳入优先审评,具体信息如下:

(资料来源:CDE)
索凡替尼是继呋喹替尼后,和黄医药自主研发并申报上市的第2个1类新药。索凡替尼是国内首个因疗效太好提前终止临床试验的创新药,用于治疗晚期非胰 腺神经内分泌瘤(NET),开启了国内靶向治疗非胰 腺神经内分泌瘤的时代。
和黄医药第2个申报上市的1类新药
索凡替尼(Surufatinib)是一种可选择性抑制与血管内皮生长因子受体(VEGFR)和成纤维细胞生长因子受体(FGFR)相关的酪氨酸激酶活性及集落刺激因子-1受体(CSF -1R)的口服候选药物,成纤维细胞生长因子受体(FGFR)是肿瘤增长中起作用的蛋白质的受体,而集落刺激因子-1受体(CSF-1R)参与阻断肿瘤相关巨噬细胞活化的信号通路,它能庇护癌细胞免受T细胞的杀伤性攻击。
索凡替尼是和黄医药第2个自主研发并申报上市的1类新药,也是和黄医药自主完成在中国的概念验证试验,并扩展到美国进行临床研究的第一个肿瘤候选药物。
疗效太好,提前终止Ⅲ期
和黄医药于2019年11月提交索凡替尼的上市申请,适应症为晚期非胰 腺神经内分泌瘤。
此次上市申请是基于成功的SANET-ep临床研究数据。
SANET-ep是一项关于索凡替尼以晚期非胰 腺神经内分泌瘤为适应症的Ⅲ期关键性研究。2019年6月,该研究独立数据监察委员会(IDMC)评估认为,共198名患者参与的中期分析成功达到无进展生存期(PFS)这一预设主要疗效终点,并提前终止研究。在国产新药中,出现疗效太好,提前终止Ⅲ期临床的,索凡替尼应该是第一个。
研究结果表明,索凡替尼使有关疾病进展或死亡率下降了67%,且总体上耐受性良好。根据研究者评估,索凡替尼治疗组患者的中位PFS为9.2个月,与之相比,安慰剂组患者则为3.8个月。在所有亚组中均观察到了索凡替尼的治疗疗效,并且这些治疗疗效得到了包括客观缓解率(ORR)、疾病控制率(DCR)、到达疾病缓解的时间(TTR)、缓解持续时间(DoR)等次要疗效终点指标的显著改善的统计数据的支持。

(资料来源:药物临床试验登记与信息公示平台)
开启了国内靶向治疗非胰 腺神经内分泌瘤的时代
神经内分泌瘤(NET)起源于与神经系统相互作用的细胞或产生激素的腺体。按照起源,神经内分泌瘤通常分为胰 腺神经内分泌瘤和非胰 腺神经内分泌瘤。与其他肿瘤相比,神经内分泌瘤患者的生存期相对较长,因此,虽然神经内分泌瘤发病率相对不高,但患者人群相对较大。
据估计,2018年美国神经内分泌瘤患者约14.1万名,其中约有超九成为非胰 腺神经内分泌瘤患者。在中国,2018年约有6.76万例神经内分泌瘤新诊断病例。按照中国的发病率与流行率比例估算,中国或有高达30万名神经内分泌瘤患者。据估计,在中国患有神经内分泌瘤的患者中约有八成是非胰 腺神经内分泌瘤患者。
目前在国内获批的靶向治疗药物包括苹果酸舒尼替尼(商品名:索坦)和依维莫司(商品名:飞尼妥),用于治疗胰 腺神经内分泌瘤或高度分化的非功能性胃肠道或肺神经内分泌瘤。
和黄医药拥有索凡替尼在全球范围内的所有权利,索凡替尼若顺利获批,将填补国内靶向治疗非胰 腺神经内分泌瘤的空白。
单药以及联用多个临床试验正在进行中
与此同时,索凡替尼的其他适应症研究也在进展中。2019年3月,和黄医药启动了一项Ⅱ/Ⅲ期临床试验,旨在对比索凡替尼和卡培他滨治疗一线化疗失败晚期胆道癌患者的疗效和安全性,主要终点为OS。
因为索凡替尼具有抗肿瘤血管生成和免疫调节的双重机制,它可能非常适合与其他免疫疗法联合使用。2018年11月-2019年9月,和黄医药达成了数个合作协议,以评估索凡替尼联合PD-1单抗的安全性、耐受性和疗效。其中包括与君实生物在全球共同开发索凡替尼与拓益联合疗法的合作协议,及与信达生物在全球共同开发达伯舒联合疗法的合作协议。
详细信息请参阅"索凡替尼报产 NET治疗领域迎来首个国产靶向新药上市申请"。
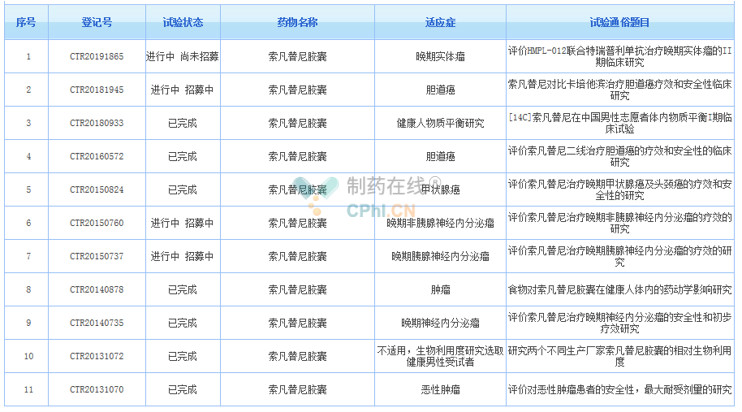
(资料来源:药物临床试验登记与信息公示平台)
获美国孤儿药资格
11月25日,和黄医药宣布索凡替尼(surufatinib)获美国FDA授予的孤儿药资格,用于胰 腺神经内分泌肿瘤(NET)治疗。如果孤儿药资格经FDA获准上市,索凡替尼对此适应症将获得为期7年的市场独占权。孤儿药资格还可在美国带来一定的开发成本收益。

(资料来源:FDA)
和黄医药研发管线

(资料来源:和黄医药官网,更新时间:2019.9.30)
作者简介:菜菜,上海交通大学药学硕士,曾工作于科学技术情报研究所,现为药监系统从业人员,擅长解读行业法规、药研动态等。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57