
近年来,以小分子靶向药物和大分子单克隆抗体类(免疫治疗药物)为代表的新型抗肿瘤药物快速涌现。为进一步规范新型抗肿瘤药物临床应用,提高肿瘤合理用药水平,保障医疗质量和医疗安全,维护肿瘤患者健康权益,国家卫生健康委组织合理用药专家委员会共同编制了《新型抗肿瘤药物临床应用指导原则》,自2018年首版发布后每年更新一次,成为目前国内可及、各专科、各种新型抗癌药物规范化使用的"标杆文件"。
2020年12月30日,最新修订的《新型抗肿瘤药物临床应用指导原则(2020年版)》在医政医管局官网正式发布,本次更新与2019版相比有哪些变化?一起来看一下。
《新型抗肿瘤药物临床应用指导原则(2020年版)》共涉及24个瘤种、115种肿瘤药;在2019版基础上新增食管癌、骨巨细胞瘤、腺泡状软组织肉瘤、透明细胞肉瘤、其他晚期软组织肉瘤和头颈部鳞状细胞癌6个瘤种,新增抗肿瘤新药适应证27个(同一药物拓展适应证重复计数)。
新药增加
呼吸系统肿瘤用药:
肺癌
新增阿美替尼(必须经基因检测携带EGFR-T790M突变),度伐利尤单抗,卡瑞利珠单抗(必须经基因检测排除EGFR突变和ALK融合变异)和阿替利珠单抗。
1. 阿美替尼 Almonertinib
制剂与规格:片剂:55mg
适应证:既往经EGFR-TKI治疗时或治疗后出现疾病进展,并且经检测确认存在EGFR-T790M突变阳性的局部晚期或转移性NSCLC成人患者的治疗。
合理用药要点:
用药前必须明确有经国家药品监督管理局批准的检测方法检测到EGFR-T790M突变。肿瘤组织和血液均可用于EGFR突变检测,组织检测优先。
2. 度伐利尤单抗 Durvalumab
制剂与规格:注射液:120mg(2.4ml)/瓶、500mg(10ml)/瓶
适应证:度伐利尤单抗适用于在接受铂类药物为基础的化疗同步放疗后未出现疾病进展的不可切除、Ⅲ期NSCLC患者的治疗。
3.卡瑞利珠单抗 Camrelizumab
制剂与规格:粉针剂:200mg/瓶
适应证:卡瑞利珠单抗联合培美曲塞和卡铂适用于EGFR基因突变阴性和ALK阴性的、不可手术切除的局部晚期或转移性非鳞NSCLC的一线治疗。
合理用药要点:
用药前必须明确诊断为EGFR突变阴性和ALK阴性的非鳞NSCLC。
4. 阿替利珠单抗 Atezolizumab
制剂与规格:注射液:1200mg(20ml)/瓶
适应证:阿替利珠单抗与卡铂和依托泊苷联合用于广泛期小细胞肺癌患者的一线治疗。
消化系统肿瘤用药:
肝癌,食管癌,胃癌,胃肠道间质瘤,胰 腺神经内分泌瘤,结直肠癌
新增卡瑞利珠单抗,帕博利珠单抗和纳武利尤单抗。
1.卡瑞利珠单抗 Camrelizumab
制剂与规格:粉针剂:200mg/瓶
适应证:
1)既往接受过一线化疗后疾病进展或不可耐受的局部晚期或转移性食管鳞癌患者治疗。
2)既往接受过索拉非尼治疗和/或含奥沙利铂系统化疗的晚期肝细胞癌患者的治疗。
2.帕博利珠单抗 Pembrolizumab
制剂与规格:注射液:100mg(4ml)/瓶
适应证:由国家药品监督管理局批准的检测评估为PD-L1综合阳性评分(CPS)≥10、既往一线全身治疗失败的局部晚期或转移性食管鳞状细胞癌。
3.纳武利尤单抗 Nivolumab
制剂与规格:注射液:40mg(4ml)/瓶、100mg(10ml)/瓶
适应证:既往接受过两种或两种以上全身性治疗方案的晚期或复发性胃或胃食管连接部腺癌患者。
血液肿瘤用药:
白血病,淋巴瘤,多发性骨髓瘤,骨髓增殖性疾病
新增维布妥昔单抗(CD30阳性),泽布替尼,达雷妥尤单抗和替雷利珠单抗。
1. 维布妥昔单抗 Brentuximab Vedotin
制剂与规格:粉针剂:50mg/瓶
适应证:复发性或难治性系统性间变性大细胞淋巴瘤(sALCL)患者。复发性或难治性经典型霍奇金淋巴瘤(cHL)患者。
美国FDA获批的其他适应证:先前接受过系统治疗的原发性皮肤间变性大细胞淋巴瘤或CD30阳性蕈样真菌病成人患者;联合化疗治疗初治Ⅲ或Ⅳ期经典型霍奇金淋巴瘤、初治系统性间变性大细胞淋巴瘤或其他表达CD30的外周T细胞淋巴瘤患者。
2.泽布替尼 Zanubrutinib
制剂与规格:胶囊:80mg
适应证:
1. 既往至少接受过一种治疗的成人套细胞淋巴瘤(MCL)患者。
2. 既往至少接受过一种治疗的成人慢性淋巴细胞白血病(CLL)/ 小淋巴细胞淋巴瘤(SLL)患者。
3.达雷妥尤单抗 Daratumumab
制剂与规格:注射液:100mg(5ml)/瓶、400mg(20ml)/瓶
适应证:单药治疗复发和难治性多发性骨髓瘤成年患者,患者既往接受过包括蛋白酶体抑制剂和免疫调节剂的治疗且最后一次治疗时出现疾病进展。
4.替雷利珠单抗 Tislelizumab
制剂与规格:注射液:100mg(10ml)/瓶
适应证:
1.至少经过二线系统化疗的复发或难治性经典型霍奇金淋巴瘤的治疗。
2.适用于PD-L1高表达的含铂化疗失败包括新辅助或辅助化疗12个月内进展的局部晚期或转移性尿路上皮癌的治疗。
泌尿系统肿瘤用药:
肾癌:新增仑伐替尼和安罗替尼。
1.仑伐替尼 Lenvatinib
制剂与规格:片剂:4mg、10mg
适应证:与依维莫司联用治疗既往接受抗血管生成药物治疗失败或进展的晚期肾细胞癌(RCC)。
2.安罗替尼 Anlotinib
制剂与规格:胶囊:8mg、10mg、12mg
适应证:本品适用于晚期RCC中高危患者的一线治疗和曾接受VEGFR-TKI治疗失败的晚期RCC患者的治疗。
合理用药要点:
CYP1A2和CYP3A4/5诱导剂(如奥美拉唑或利福平)可能降低本品的血浆浓度,建议避免与CYP1A2和CYP3A4的抑制剂及诱导剂合用。
乳腺癌用药:
乳腺癌:新增恩美曲妥珠单抗(HER2阳性:IHC3+,FISH阳性或基因检测HER2扩增),伊尼妥单抗(HER2阳性:IHC3+,FISH阳性或基因检测HER2扩增),奈拉替尼(HER2阳性:IHC3+,FISH阳性或基因检测HER2扩增)和西达本胺。
1.恩美曲妥珠单抗 Trastuzumab Emtansine(T-DM1)
制剂与规格:针剂:100mg/瓶、160mg/瓶
适应证:单药适用于接受了紫杉类联合曲妥珠单抗为基础的新辅助治疗后仍残存侵袭性病灶的HER2阳性早期乳腺癌患者的辅助治疗。
合理用药要点:
接受T-DM1辅助治疗的患者应在有资质的病理实验室通过HER2检测确认为HER2阳性(HER2阳性的定义为IHC3+和/或FISH阳性)。
2.伊尼妥单抗 Inetetamab
制剂与规格:针剂:50mg/支
适应证:本品适用于HER2阳性,与长春瑞滨联合治疗已接受过1个或多个化疗方案的转移性乳腺癌患者。
合理用药要点:
在接受伊尼妥单抗治疗前,应在有资质的病理实验室进行 HER2 检测,HER2 阳性患者方可应用伊尼妥单抗治疗。
3.奈拉替尼 Neratinib
制剂与规格:片剂:40mg
适应证:适用于HER2阳性的早期乳腺癌成年患者,在接受含曲妥珠单抗辅助治疗之后的强化辅助治疗。
合理用药要点:
用药前必须明确有经国家药品监督管理局批准的检测方法检测到EGFR-T790M突变。肿瘤组织和血液均可用于EGFR突变检测,组织检测优先。
4.西达本胺 Chidamide
制剂与规格:片剂:5mg
适应证:联合芳香化酶抑制剂用于HR阳性、HER2阴性、绝经后、经内分泌治疗复发或进展的局部晚期或转移性乳腺癌患者。
合理用药要点:
用药前必须明确有经国家药品监督管理局批准的检测方法检测到EGFR-T790M突变。肿瘤组织和血液均可用于EGFR突变检测,组织检测优先。
皮肤肿瘤用药:
黑色素瘤:新增达拉非尼(必须经基因检测携带BRAF V600突变)和曲美替尼(必须经基因检测携带BRAF V600突变)。
1.达拉非尼联合曲美替尼
制剂与规格:达拉非尼胶囊:50mg、75mg;曲美替尼片剂:0.5mg、2mg。
适应证:
1)达拉非尼联合曲美替尼适用于治疗BRAF V600突变阳性的不可切除或转移性黑色素瘤患者。
2)达拉非尼联合曲美替尼适用于BRAF V600突变阳性的Ⅲ期黑色素瘤患者完全切除后的辅助治疗。
合理用药要点
本品联合曲美替尼治疗前须经国家药品监督管理局批准的检测方法进行BRAF V600突变检测,确认为BRAF V600突变阳性的患者方可接受本品治疗。本品联合曲美替尼不适用于BRAF野生型黑色素瘤患者。
骨与软组织肿瘤用药:
结节性硬化症相关的室管膜下巨细胞星形细胞瘤,结节性硬化症相关的肾血管平滑肌脂肪瘤,骨巨细胞瘤,腺泡状软组织肉瘤,透明细胞肉瘤和其他晚期软组织肉瘤;
新增地舒单抗和安罗替尼。
1.地舒单抗 Denosumab
制剂与规格:注射液:120mg(1.7ml)/瓶
适应证:治疗不可手术切除或者手术切除可能导致严重功能障碍的骨巨细胞瘤(GCTB),包括成人和骨骼发育成熟(定义为至少一处成熟长骨且体重≥45 kg)的青少年患者。
肉瘤:
1.安罗替尼 Anlotinib
制剂与规格:胶囊:8mg、10mg、12mg
适应证:适用于腺泡状软组织肉瘤(ASPS)、透明细胞肉瘤(CCS)以及既往至少接受过含蒽环类化疗方案治疗后进展或复发的其他晚期软组织肉瘤(STS)患者的治疗。
合理用药要点:
建议安罗替尼避免与CYP1A2和CYP3A4/5的强抑制剂及强诱导剂合用。
头颈部肿瘤用药:
鼻咽癌,甲状腺癌,头颈部鳞状细胞癌;
新增纳武利尤单抗和西妥昔单抗(EGFR表达)。
1.纳武利尤单抗 Nivolumab
制剂与规格:注射液:40mg(4ml)/瓶、100mg(10ml)/瓶
适应证:本品适用于治疗接受含铂类方案治疗期间或之后出现疾病进展且肿瘤PD-L1表达阳性(定义为表达PD-L1的肿瘤细胞≥1%)的复发性或转移性头颈部鳞状细胞癌(SCCHN)患者。
合理用药要点
对于接受含铂类方案治疗期间或之后出现疾病进展且肿瘤PD-L1表达阳性(定义为表达PD-L1的肿瘤细胞≥1%)的复发性或转移性头颈部鳞状细胞癌患者。
2. 西妥昔单抗 Cetuximab
制剂与规格:注射液:100mg(20ml)/瓶
适应证:本品用于治疗头颈部鳞状细胞癌:与铂类和氟尿嘧啶化疗联合用于一线治疗复发和/或转移性疾病。
合理用药要点:
本品与铂类化合物为基础的化疗药物联合应用于复发和/或转移性头颈部鳞状细胞癌的治疗,随后继续使用本品进行维持治疗,直至疾病进展。化疗药物的使用必须在本品滴注结束1小时之后开始。
无论EGFR的表达状况如何,所有有效性终点均证实有临床获益。尚无证据证实EGFR表达等相关标志物检测能预测本品在头颈部鳞状细胞癌患者中的疗效。
生殖系统肿瘤用药:
卵巢癌:新增尼拉帕利。
1.尼拉帕利 Niraparib
制剂与规格:胶囊:100mg
适应证:铂敏感的复发性上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者在含铂化疗达到完全缓解或部分缓解后的维持治疗。
合理用药要点:
本品通过羧酸酯酶进行代谢,在与CYP诱导剂和CYP抑制剂合并使用时,不需要调整剂量。
该《原则》还新增了"免疫相关性不良反应和治疗调整方案"和"反应性毛细血管增生症分级标准和治疗建议",更加注重免疫治疗在临床上面的不良反应管理。
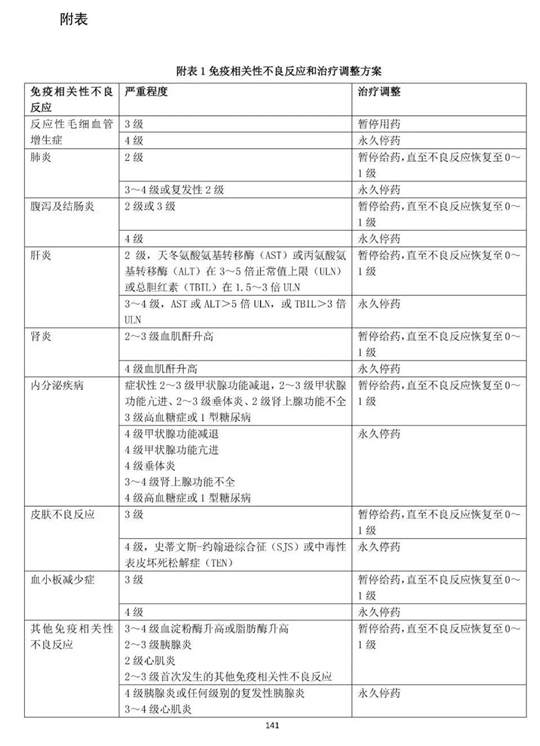
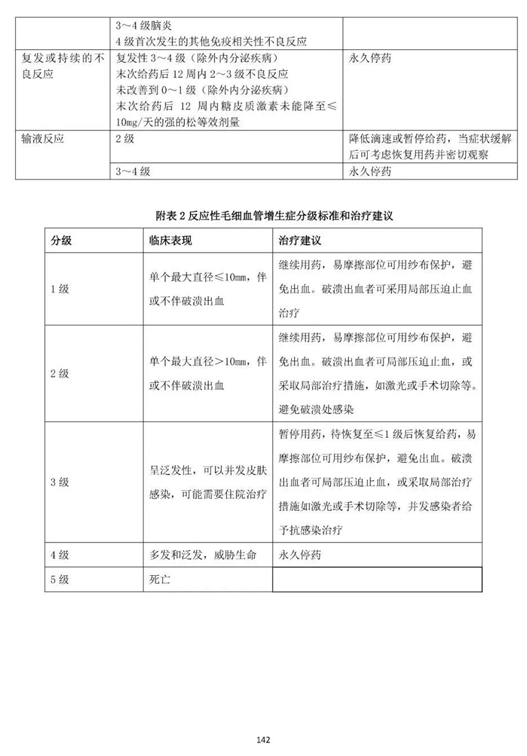
参考:
《新型抗肿瘤药物临床应用指导原则(2020年版)》;
《新型抗肿瘤药物临床应用指导原则(2019年版)》。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57