近日,医学界迎来一大突破——首 个针对实体瘤的细胞疗法正式获得批准并上市。2月16日,美国生物技术公司Iovance Biotherapeutics报告称,FDA已快速通过了对AMTAGVI™(lifileucel)的生物制品许可申请(BLA)。Lifileucel作为一种肿瘤浸润淋巴细胞(TIL)疗法,专为那些在接受PD-1/PD-L1治疗后仍出现病情进展的晚期黑色素瘤患者设计。值得一提的是,lifileucel成为全球首 个获得批准上市的TIL细胞疗法,标志着肿瘤治疗领域的一个新的里程碑。此疗法经过严格的临床试验与评估,被认为能够有效对抗多种实体瘤疾病,为广大癌症患者带来了新的治疗希望。此项技术的诞生,不仅代表了生物技术领域的又一巨大飞跃,更可能成为未来癌症治疗领域的指引灯塔。国际知名学术期刊Nature对此也给予了高度评价,称其为癌症治疗的新里程碑。
这一创新疗法,旨在利用细胞治疗技术的独特性能,直接针对肿瘤组织进行精确打击,旨在减少副作用、提高治疗效果。经过深入研究和临床试验,该细胞疗法在安全性和有效性方面均表现出色,为众多实体瘤患者带来了前所未有的治疗选择。
Nature杂志在其报道中明确指出,这一细胞疗法的获批上市,标志着癌症治疗进入了新的历史阶段。这一里程碑式的进展标志着免疫细胞疗法开始显现出治疗实体瘤的临床价值;此前,CAR-T等细胞疗法已被成功应用于血液系统恶性肿瘤。

图表来源:参考资料[1]
一、TIL细胞疗法:原理与操作流程的深入探讨
原理概述:
TIL(Tumor-Infiltrating Lymphocytes)细胞疗法是一种利用患者体内的抗肿瘤免疫反应来对抗恶性肿瘤的前沿疗法。这种方法的核心在于提取并扩增患者肿瘤组织中的浸润淋巴细胞(TILs),这些细胞已经在肿瘤微环境中被激活并具有特定的抗肿瘤活性。通过体外培养和扩增,可以进一步增强TILs的抗肿瘤效果,并将它们重新注入患者体内,以攻击和消除肿瘤细胞。
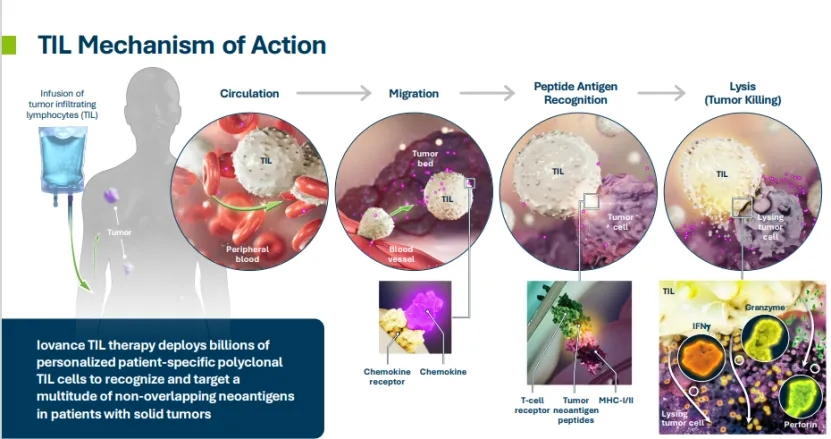
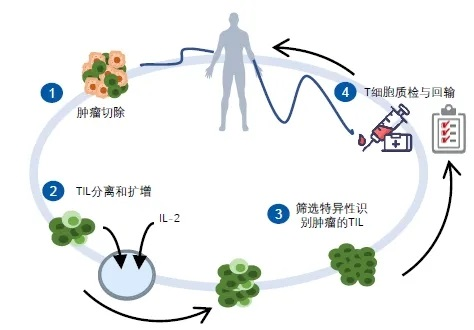
流程详解:
1. 样本采集与处理:首先从患者的肿瘤组织中采集细胞样本。这个过程通常通过微创手术或活检完成,以确保获得足够数量和质量的细胞。采集后的细胞需要立即进行处理,以保持其活力和功能性。
2. 细胞分离与培养:在采集的细胞样本中,通过先进的细胞分离技术,如流式细胞仪,将TILs从中分离出来。然后,在特定的培养基和条件下,对分离出来的TILs进行体外培养。这个过程通常需要特定的营养成分、细胞因子和其他生物活性物质来支持细胞的生长和扩增。
3. 细胞扩增:经过数天的培养,TILs的数量将显著增加。这个过程中,细胞会经历多轮的分裂和增殖,从而达到治疗所需的细胞数量。为确保细胞的质量和功能,扩增过程中需要进行严格的细胞活性和纯度检测。
4. 治疗准备:扩增完成后,这些经过改造和增强的TILs将被用于治疗。在治疗前,医生会根据患者的具体情况,制定个性化的治疗方案,包括细胞注射的剂量、时间和方式等。
5. 细胞回输:最后,经过扩增的TILs将通过静脉注射等方式重新注入患者体内。这些细胞将在患者体内继续发挥其抗肿瘤作用,通过直接攻击和消灭肿瘤细胞,以及激发体内的免疫反应,共同对抗癌症。
与CAR-T细胞疗法类似,TIL细胞疗法也是过继性免疫治疗的一种形式。这种方法从患者的肿瘤组织中提取出浸润的淋巴细胞,然后在体外进行大量的扩增,最后再将这些细胞回输给患者。由于这些细胞具有患者抗原特异性,因此它们能够精确地识别并攻击患者的癌细胞,从而达到治疗的效果。
二、振奋人心的临床研究结果
这次加快的审批过程是基于lifileucel对晚期黑色素瘤患者的II期临床试验C-144-01所得到的积极结果。在C-144-01研究中,参与的患者主要是那些之前已经接受过至少一次全身治疗,包括PD-1抗体,但病情仍然处于不可切除或转移性状态的黑色素瘤患者。若患者被诊断为BRAF V600突变阳性,则需要同时接受BRAF抑制剂与MEK抑制剂的联合治疗。
C-144-01是一场开放式的、涉及多队列及多中心的2期临床试验,其核心目标在于探索单次注射lifileucel在晚期黑色素瘤患者中的治疗效果和安全性。这些患者均在接受PD-1/PD-L1抑制剂治疗期间或之后病情出现了进展。根据已公布的研发成果表明,lifileucel的治疗效果持久且具备良好的安全性。当中位随访时间设定为27.6个月时,对于那些经过大量预治疗(中位治疗线数:3)的患者,由独立审评委员会(IRC)评估的客观缓解率(ORR)达到了31.4%(95% CI:23.5-47.6)。其中,有8位患者实现了完全缓解(CR),40位患者实现了部分缓解(PR)。这一成果为lifileucel在未来黑色素瘤治疗领域的应用提供了有力支持。
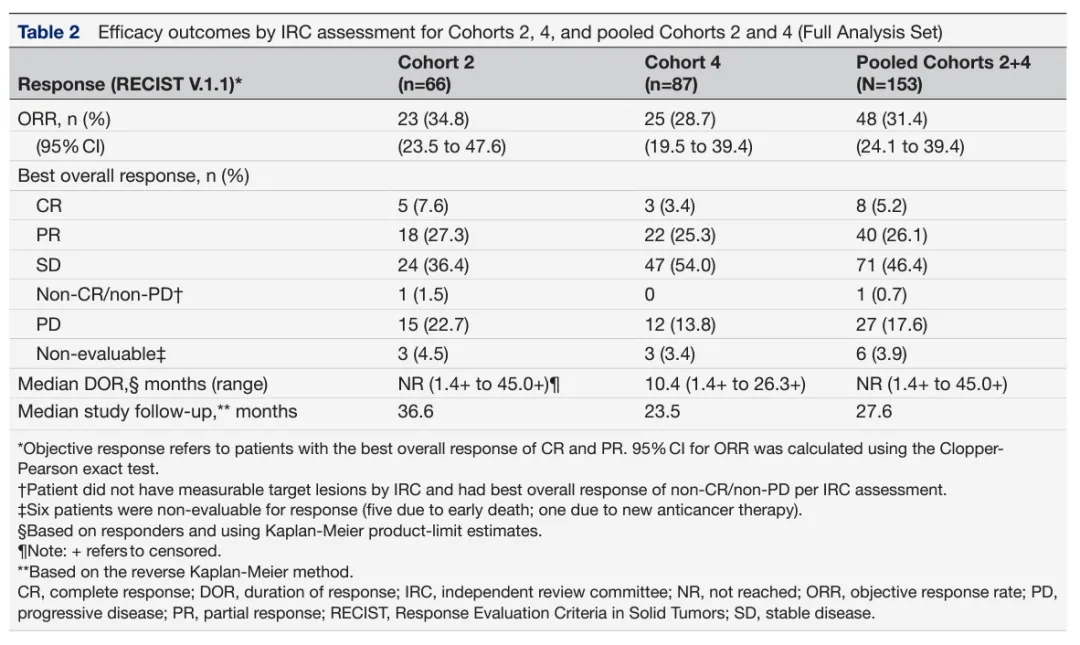
Lifileucel在中位随访27.6个月时的疗效结果摘要(图表来源:参考资料[4])
lifileucel在治疗过程中展示出了显著且持久的疗效。主要疗效分析所涵盖的73名患者,是从指定的生产厂接受推荐剂量的lifileucel的群体。在这些患者中,有31.5%的患者根据实体瘤应答评价标准(RECIST 1.1)实现了客观缓解。进行了18.6个月的随访后,发现其中位缓解持续时间仍未达到上限,且有43.5%的患者的缓解持续时间超过了12个月。此外,综合疗效集的数据则包括了来自队列4和队列2的共计153名患者。在这153名患者中,有31.4%的患者通过RECIST 1.1标准达到了客观缓解。经过21.5个月的随访,这些患者的中位缓解持续时间也尚未达到上限,且有54.2%的患者的缓解持续时间超过了12个月。
经过与FDA的深入讨论,Iovance公司成功敲定了lifileucel药物的III期注册试验(代号为TILVANCE-301)的设计方案。该试验的核心内容在于探索lifileucel与K药的联合疗法在针对一线晚期黑色素瘤治疗效果。研究的主要目标是为了全面支撑lifileucel在PD-1单抗治疗无效后的黑色素瘤患者中的应用,并期望为lifileucel与K药联合在一线晚期黑色素瘤治疗方案中的注册申请提供坚实依据。
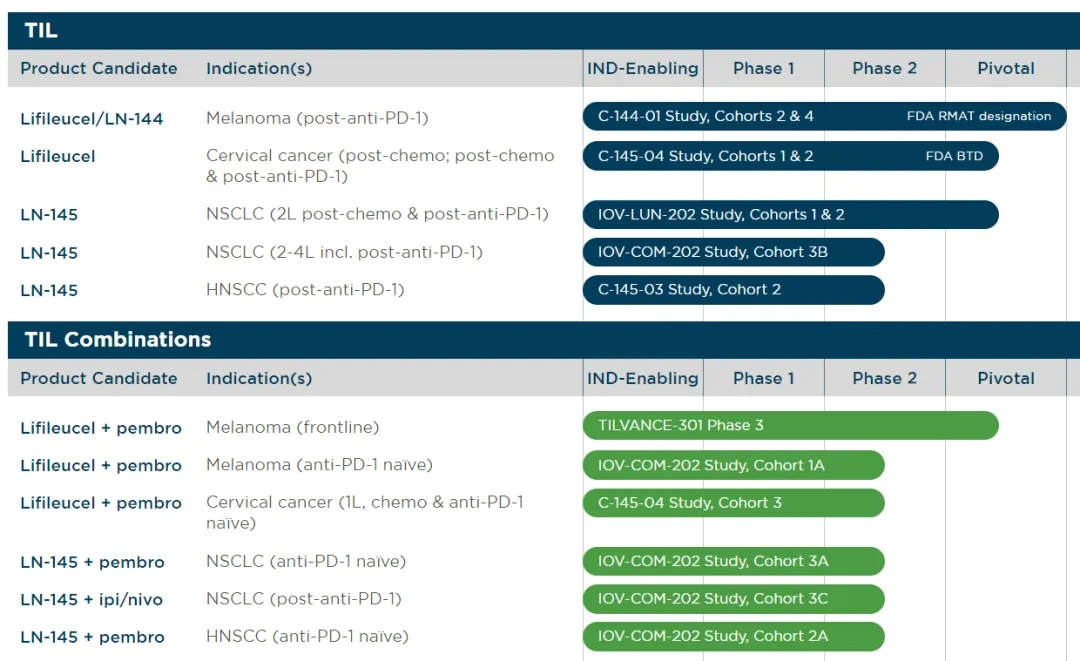
Iovance旗下lifileucel相关管线图(图表来源:Iovance Biotherapeutics公司官网)
三、lifileucel副反应
在经过前序化疗与IL-2治疗后,采用TIL疗法可能出现如贫血、发热等常见副作用。此外,还存在风险,即TILs可能误攻击正常细胞,从而诱发白癜风等自身免疫性问题。
与CAR-T细胞类似,TILs的个体化特征极为明显。由于每位患者的TILs所识别的抗原各不相同,因此它们在体内的效应也相对独立。
Iovance公司所获得的批准是基于FDA对TILs的增殖工艺及给药流程的严格审核与认证,而并非仅仅基于特定的细胞类型。值得一提的是,TILs的天然非专利性特点为其工艺的不断改进与优化提供了极大的便利。
四、TIL疗法巨大成本与投资未来潜力
Iovance公司推出的lifileucel单次疗程定价高达51.5万美元,这比市面上部分CAR-T疗法的价格还要昂贵。然而,值得注意的是,包括丹麦哥本哈根大学医院在内的多家大学附属机构已经以较低成本(约5.5万美元)成功地实施了TIL疗法来治疗
经典的CAR-T疗法曾备受推崇,但其应用主要局限于血液科癌症,在实体瘤治疗中屡遭挫折。然而,令人振奋的是,CAR-T疗法在自身免疫性疾病的治疗中取得了新的突破。更值得一提的是,TILs细胞疗法已首次获批用于治疗实体瘤,这标志着医疗领域的一大进步。医生科学家们通过不懈努力,逐步推动着医疗技术的发展。
Iovance公司的lifileucel获批上市意义重大,它创新性地证明了TILs治疗部分实体瘤的有效性,从而鼓舞着其他类似公司继续拓展细胞疗法的应用领域。目前,TIL疗法正在针对一系列实体瘤进行研究和开发,其中包括宫颈癌和肺癌,这两种癌症在临床试验中已经显示出了一定的治疗效果。未来,通过基因改造等手段,我们有望进一步增强TILs的浸润与杀伤能力,并通过阻断癌细胞对TILs的反制信号通路,实现患者的完全缓解。
尽管Iovance公司面临着与其他CAR-T研发公司相同的困境,即个体化治疗流程的制约,但TILs细胞疗法的批准仍为该公司带来了喜讯。然而,TILs的未来应用很可能取决于医疗机构自主开发的TIL疗法中心。
目前,许多创新型企业正致力于推动TIL疗法的进步,并已研发出多款进入临床试验阶段的疗法。优化TIL疗法的一个重要策略是从中筛选出抗癌活性最强的细胞亚型进行扩增。TIL包含多样的T细胞克隆,各自具有独特的免疫特性和靶向不同的癌症抗原的能力。作为TIL领域的先驱,Steven Rosenberg博士透露,第一代TIL疗法中仅有三分之一的细胞在与肿瘤细胞共培养时能有效识别肿瘤细胞。“大部分注入患者体内的细胞并不具备活性,”他强调,“因此,选择具备理想特征的细胞将极大地提升治疗效果。
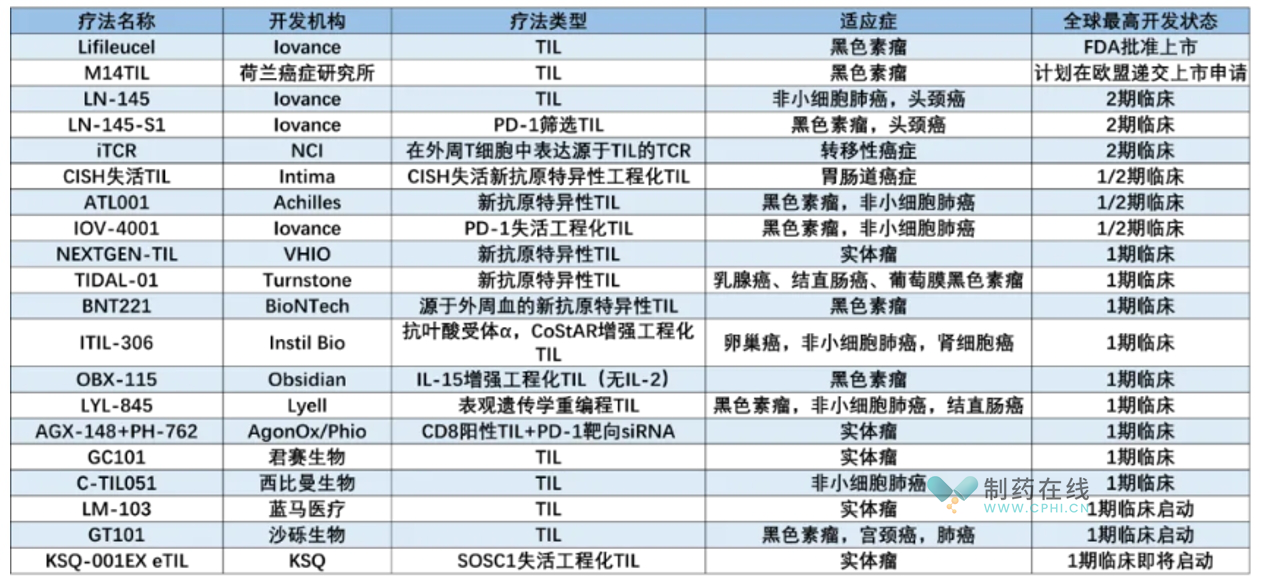
部分在研TIL疗法(数据来源:参考资料[6] &公开资料)
另一种策略则集中在利用基因工程来优化TIL细胞的功能,增强其对抗癌症的效果。举例来说,借助先进的基因编辑技术,可以使PD-1受体的表达得到抑制,这样一来,TIL细胞在肿瘤微环境中就不易受到PD-L1的制约,从而更好地发挥其抗癌活性。除此之外,其他的基因编辑目标可能包括CISH这一免疫检查点蛋白,以及抑制细胞因子信号的SOCS1等。这些基因工程的改造举措有望进一步提升TIL细胞的扩增和植入效率,从而拓展其应用领域,使更多的癌症患者受益于这种治疗方法。
全球每年约有32.5万新发黑色素瘤患者,其中约有5.7万患者因此病而死亡。而在美国,每年约有10万人被诊断出患有黑色素瘤,约有7700人因此病致死。随着FDA的批准,TIL疗法将成为晚期黑色素瘤治疗的全新选择。
参考文献:
[1]https://www.fda.gov/drugs/resources-information-approved-drugs/fda-grants-accelerated-approval-lifileucel-unresectable-or-metastatic-melanoma
[2]https://www.nature.com/articles/d41586-024-00673-w
[3] Iovance’s AMTAGVI (lifileucel) Receives U.S. FDA Accelerated Approval for Advanced Melanoma. Retrieved February 16, 2024 from https://www.globenewswire.com/news-release/2024/02/16/2830923/0/en/Iovance-s-AMTAGVI-lifileucel-Receives-U-S-FDA-Accelerated-Approval-for-Advanced-Melanoma.html
[4] Chesney J, Lewis KD, Kluger H, Hamid O, Whitman E, Thomas S, Wermke M, Cusnir M, Domingo-Musibay E, Phan GQ, Kirkwood JM, Hassel JC, Orloff M, Larkin J, Weber J, Furness AJS, Khushalani NI, Medina T, Egger ME, Graf Finckenstein F, Jagasia M, Hari P, Sulur G, Shi W, Wu X, Sarnaik A. Efficacy and safety of lifileucel, a one-time autologous tumor-infiltrating lymphocyte (TIL) cell therapy, in patients with advanced melanoma after progression on immune checkpoint inhibitors and targeted therapies: pooled analysis of consecutive cohorts of the C-144-01 study. J Immunother Cancer. 2022 Dec;10(12):e005755. doi: 10.1136/jitc-2022-005755. PMID: 36600653; PMCID: PMC9748991.
[5] LONG-TERM EFFICACY AND PATTERNS OF RESPONSE OF LIFILEUCEL TUMORINFILTRATING LYMPHOCYTE (TIL) CELL THERAPY IN PATIENTS WITH ADVANCED MELANOMA: A 4-YEAR ANALYSIS OF THE C-144-01 STUDY. Retrieved January 15, 2024 fromhttps://www.iovance.com/uploads/ESMO-IO-C-144-01-4-year-2577-publication.pdf
[6] Asher Mullard. (2023). Tumour-infiltrating lymphocyte cancer therapy nears FDA finish line. Nature Reviews Drug Discovery, doi: https://doi.org/10.1038/d41573-023-00206-6



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57