
2025年3月19日,国家药监局发布《药品试验数据保护实施办法(试行)》征求意见稿,这场筹备七年的制度改革正式拉开帷幕。数据显示,2020-2024 年国内公立医疗机构药品销售中,仿制药占比高达 70%,而创新药仅占 30%。政策设计者瞄准这一结构性矛盾,通过建立分层数据保护机制,为创新药研发注入 "强心剂"。
此次改革与国际通行的 ICH 标准深度接轨,明确境外原研药若在境内同步申报,数据保护期可扣除境内外审批时间差。这一设计直接推动跨国药企将中国纳入全球研发首梯队,某 PD-1 抑制剂在 2024 年实现中美同步获批,其中国区市场份额当年突破 15%,印证了政策的磁吸效应。

一、分层保护的 "三驾马车" 设计
政策创造性地构建三级保护体系:创新药 6 年、改良型新药 3 年、首仿药 3 年。这种差异化策略精准匹配不同创新层级需求,既避免 "躺平式仿制",又防止过度垄断。以某儿童用药改良剂型为例,获批后凭借 3 年保护期迅速占领细分市场,带动企业研发管线中儿童药占比提升至 35%。
数据来源:国家药监局
首仿药保护机制尤为关键。对境外已上市、境内未上市药品的首家仿制药给予 3 年保护,迫使企业从 "逆向工程" 转向自主临床试验。2024 年某罕见病仿制药通过自主研发获得批准,价格较原研药降低 72%,填补 国内空白的同时,推动企业研发投入增长 180%。
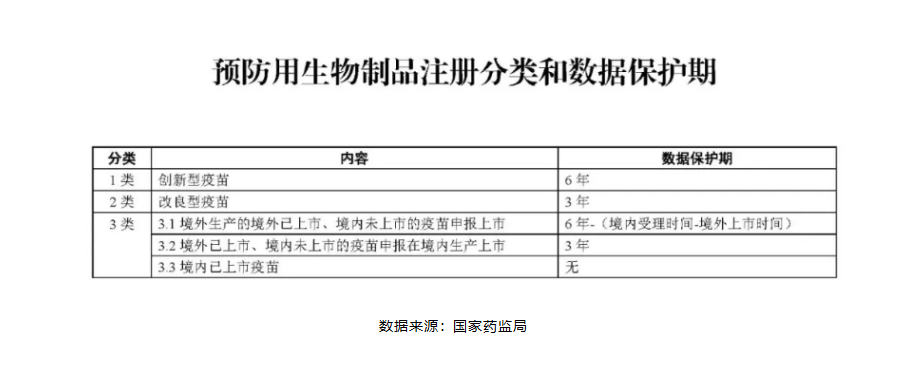
数据来源:国家药监局
数据保护与专利制度形成 "接力保护":当专利到期后,数据保护仍能提供市场独占期。2023 年某糖尿病创新药专利到期后,凭借剩余 2 年数据保护期,市场份额仍保持行业前三,研发投入回报率较传统模式提升 40%。这种机制使创新药企研发投入占比从 2018 年的 12% 跃升至 2024 年的 21%,形成 "创新有回报、仿制有空间" 的良性生态。

数据来源:国家药监局
二、【产业生态重构】创新与仿制的 "共生进化" 之路
政策红利催生出 "中国速度":某 ADC 药物从立项到获批仅用 32 个月,较传统流程缩短 14 个月;临床试验默示许可周期压缩至 45 天,生物等效性试验实现备案制。跨国药企加速布局中国研发中心,2024 年新增 5 个全球研发枢纽落地,中国区研发投入占比提升至全球 25%。
支付端改革同步推进,丙类目录探索商业保险衔接,预计 2030 年商业健康保险覆盖人群将突破 5 亿。某创新药通过医保动态调整机制,从获批到纳入目录的时间较五年前减少 40%,患者可及性显著提升。
面对数据保护壁垒,仿制药企加速向 "高端仿制 + 自主创新" 转型。武汉同济医药构建中药材种植 - 原料药生产全产业链,2023 年原料自给率提升至 75%,仿制药一致性评价通过率达 92%,高于行业平均水平 15 个百分点。其自主研发的鼻喷雾剂通过优先审评通道获批,上市 6 个月销售额破 2 亿元。
中国仿制药产业正从 "低价竞争" 转向 "技术出海"。2024 年制剂出口额突破 300 亿美元,同比增长 27%,覆盖全球 120 多个国家。某糖尿病仿制药通过自主研发获得批准,价格较原研药降低 65%,验证了 "以仿促创" 模式的可行性。
专利链接制度与数据保护形成 "组合拳"。某抗肿瘤药物专利纠纷通过早期解决机制化解,仿制药上市时间较传统诉讼模式缩短 18 个月,患者用药可及性与企业利益实现双赢。国家药监局建立的 "研发服务包" 制度,为企业提供从靶点选择到商业化的全链条指导,某 ADC 药物从立项到获批仅用 32 个月,较传统流程缩短 14 个月。
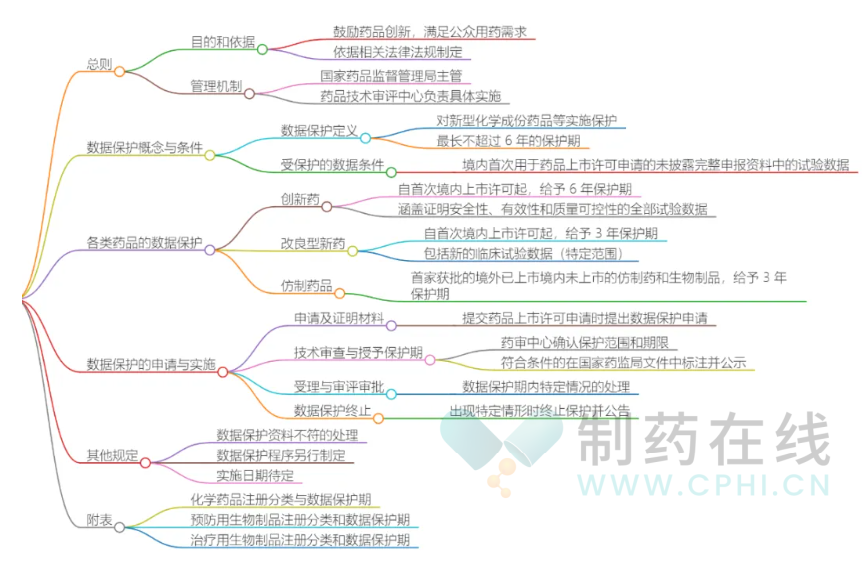
公众号:CPHI制药在线整理
三、【企业样本观察】不同赛道的破局之道
跨国药企加速融入中国创新生态。某跨国药企中国区创新药管线占比提升至 40%,2024 年在中国市场销售额同比增长 120%。其研发中心与本土 CRO 企业合作,将临床试验入组效率提升 40%,推动多个创新药实现全球同步开发。
中国生物制药 2024 年研发投入达 50.9 亿元,占营收 17.6%,其中 78% 投向创新药。6 款创新药获批上市,创新产品收入突破 120 亿元,占比 41.8%。企业通过布局抗体药物、基因治疗等前沿领域,推动从 "仿创结合" 向 "源头创新" 跨越。
互联网医疗企业凭借数据优势切入医药研发。某平台通过 AI 辅助靶点筛选,将药物发现周期缩短 30%;资本持续涌入创新药领域,2024 年融资额突破 800 亿元,推动 10-15 个创新药在欧美同步上市。
四、【未来十年展望】从 "跟随者" 到 "规则制定者"
中国正从规则接受者转变为制定参与者。2025 年计划新增 50 个国际多中心临床试验,推动 10-15 个创新药在欧美同步上市。ICH 技术标准本土化实施进度达 92%,某创新药通过 ICH Q1 稳定性指南验证,加速进入欧盟市场。
支付改革形成 "基本医保 + 普惠保险 + 高端商保" 多层次保障。2024 年动态调整药品目录,新增 91 种药品中 38 种为 "全球新" 创新药。丙类目录探索商业保险衔接,预计 2030 年商保覆盖人群突破 5 亿,特药险产品年增速超 60%。
数据侵权监管力度持续加强,2024 年专利挑战成功率提升至 63%。建立可互换目录,实现仿制药与原研药同标准支付,保障患者用药可及性。面对原料价格波动,企业通过纵向整合供应链,有效对冲成本压力,推动产业可持续发展。
这场变革的深意在于构建 "创新有回报、仿制有空间" 的生态系统。当数据保护成为创新的 "安全网",当仿制药升级成为产业的 "稳定器",中国医药产业有望在未来十年实现从 "制造大国" 到 "创新强国" 的历史性跨越。正如某跨国药企中国区负责人所言:"中国正在成为全球创新的策源地,而数据保护制度的完善,让我们更有信心在这里播撒创新的种子。"
参考来源:https://www.nmpa.gov.cn/xxgk/zhqyj/zhqyjyp/20250319181537196.html?type=pc&m=



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57