近日,恒瑞医药旗下1类**新药注射用甲苯磺酸瑞马唑仑的上市申请办理状态已变为"在审批",这款重磅**新药即将国内获批上市。

资料来源:CDE
2018年首个报产的国产新药
恒瑞医药注射用甲苯磺酸瑞马唑仑属于苯二氮卓类,是一种短效的 GABAa 受体激动剂,适用于择期手术中的全身**。
2018年3 月,恒瑞甲苯磺酸瑞马唑仑的国内上市申请获得CDE承办受理,受理号 CXHS1800002,这是2018 年国内首个申报生产的1类新药。同年4 月,甲苯磺酸瑞马唑仑凭借与现有治疗手段相比具有明显治疗优势被纳入到CDE的优先审评名单中。在2019年即将结束之际,这款新药即将在国内获批上市。
青出于蓝
瑞马唑仑的原研药物由Paion AG公司开发,该药物结合了咪 达 唑 仑的安全性与异丙酚的有效性,用于手术中的全身**。2012年,Paion公司与人福药业达成了合作协议,前者以300万欧元以及后续销售分成授予了后者瑞马唑仑在中国的开发权利。2018年11月,宜昌人福药业国内提交了1类新药注射用苯磺酸瑞马唑仑的上市申请,目前处于在审评审批中。
从原研药的专利布局来看,Paion公司瑞马唑仑原研专利短效苯并二氮杂盐及其多晶型的中国申请日为2007年7月10日,申请号为CN201310166860,公开日为2015年7月15日,公开号为CN103288834B。瑞马唑仑的游离碱不稳定,Paion公司开发的为瑞马唑仑的苯磺酸盐。
彼时的恒瑞对瑞马唑仑这款**大品种进行了有效的情报分析,找到了这款产品的漏洞,并迅速推出了改良盐型即甲苯磺酸瑞马唑仑,抢先人福医药于2018年3月在国内率先申报生产。对比瑞马唑仑的这两款盐剂型,甲苯磺酸瑞马唑仑的稳定性更高,起效更快,恒瑞医药青出于蓝。
国内临床
在药物临床试验登记与信息公示平台公示的信息中,甲苯磺酸瑞马唑仑的临床试验共计8项,其中7项已完成,包括了3项Ⅰ期临床试验、2项Ⅱ期临床试验与3项Ⅲ期临床试验,适应症覆盖了全身**、结肠镜诊疗镇静、胃镜诊疗镇静、择期全麻手术及镇静**等。
**业务板块
目前,在国内**药品市场的占有率为 11.63%,位列第二。
2018 年,恒瑞医药旗下**产品板块营收46.526亿元,同比增长29.25%,**药是恒瑞医药的三大核心业务板块之一,已成为恒瑞收入增长的主要来源之一。目前,国内**药市场的前三强依次为恒瑞医药、阿斯利康、费森尤斯。样本医院数据显示,恒瑞医药在国内**市场的占有率为25.5%,超过阿斯利康近10个百分点。
目前,恒瑞**药三大品种顺苯磺酸阿曲库铵、七氟烷和右美托咪定的年销售额均超过10亿元,甲苯磺酸瑞马唑仑有望接棒,成长为临床必需的大品种,成为下一款10亿级别重磅**产品。
除了即将获批的甲苯磺酸瑞马唑仑之外,恒瑞在研**产品管线中的M6G、SHR0410、美洛昔康及SHR8554等产品储备丰富,都是未来公司业绩的潜在利润增长点。
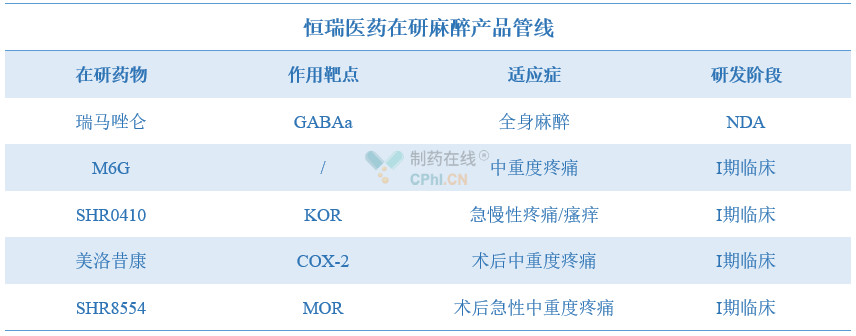
资料来源:公开资料整理
作者简介:小药丸,制药行业从业者,自媒体时代的文字搬运工,专注于制药圈内的阴晴冷暖。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57