2021年1月15日,国家药品监督管理局药品审评中心官网发布《中药新药质量研究技术指导原则(试行)》,自发布之日2021年1月15日起实施,此指南为鼓励中药传承创新发展,落实《药品管理法》、《中医药法》、《中共中央、国务院关于促进中医药传承创新发展的意见》等文件**,目前,我国尚未有专门的中药新药质量研究技术指导原则,该指导原则的正式实施将填补国内中药新药质量研究的一大空白,助力国内中药质量的进一步提升,本文为大家梳理了本指导原则中质量研究重点内容并结合自己的解读与大家分享。
一、中药新药质量研究难点
质量研究是中药新药研究的重要内容,对生产过程控制、确定药品关键质量属性、建立质量标准和保障药品质量稳定可控具有重要意义。中药多成份复杂体系的特点,目前,我国尚未有专门的中药新药质量研究技术指导原则,为进一步规范和指导中药新药质量研究,满足药品安全、有效、质量可控的要求,促进中药产业高质量发展,中药新药质量研究应在中医药理论指导下,根据中药特点、新药研发的一般规律及不同研究阶段的主要目的,开展针对性研究,落实药品全生命周期管理,促进中药传承与创新,保证药品安全、有效、质量可控,在研发过程中,药学研究要能够支持安全性和有效性研究的开展,同时不断积累药物信息,为上市时建立完善的质量控制体系提供数据支持。为坚持守正创新,CDE自2018年5月召开启动会,确定指导原则的基本框架和基本要求,明确撰写工作分工等,历经多次专家会议讨论,形成征求意见稿,2020年9月1日上网征求意见一个月(2020年10月01日截止);2021年1月15日CDE正式发布实施《中药新药质量研究技术指导原则(试行)》(成文时间为2021年1月14日),该指导原则强调中药新药质量研究应遵循五个原则:
原则一:遵循中医药理论指导。
原则二:传统质量控制方法与现代质量研究方法并重;
原则三:以药用物质基础为重要研究内容。
原则四:以保证安全有效、质量可控为目标。
原则五:贯穿药品全生命周期。
二、中药新药质量研究重点内容
质量研究的目的是确定质量控制指标和可接受范围,为药品生产过程控制和质量标准建立提供依据,保证药品的安全性、有效性和质量可控性。本指导原则明确中药新药质量研究还应体现质量源于设计、全过程质量控制和风险管理的理念,通过对药材/饮片、中间体(中间产物)、制剂的药用物质及关键质量属性在不同环节之间的量质传递研究,以及药用物质与辅料、药包材相互影响的研究,不断提高中药的质量控制水平,为中药新药质量研究提供参考。
1、药材/饮片

2、中间体

3、制剂

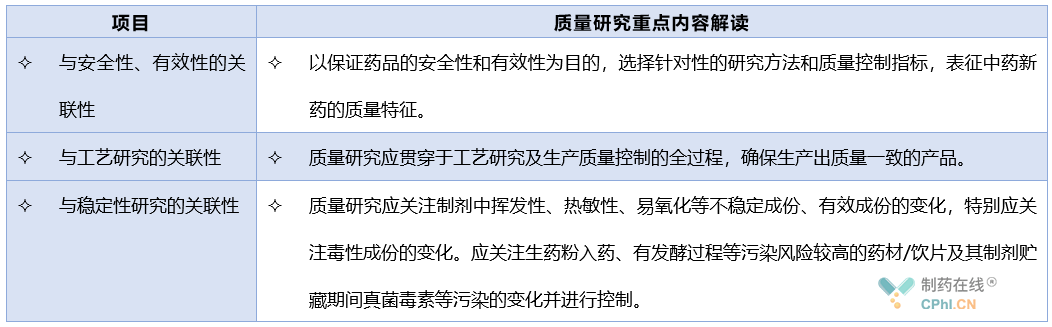
4、质量研究的关联性
参考文献
[1] http://www.cde.org.cn
作者简介:滴水司南,男,生物医药高级工程师,立足于生物医药行业质量管理工作,专注于生物医药产业。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57