随着粤港澳大湾区医疗协同发展的深入推进,临床急需港澳药品的跨境使用已成为保障居民用药需求的重要途径。然而,药品从采购到召回的全流程涉及十余个关键环节,任一环节的管理疏漏均可能引发用药安全风险、法律合规隐患甚至公共健康事件。为深化粤港澳大湾区医疗合作,规范内地九市进口港澳药品管理,满足临床急需用药需求,提升药品管理科学化与规范化水平,基于2025年2月11日广东省药学会官网重磅发布的《广东省粤港澳大湾区内地九市进口港澳药品管理专家共识》(粤药会〔2025〕26号),本文梳理了急需港澳药品在采购、验收、储存、发放、调配等全生命周期中的潜在风险点,并针对性提出覆盖供应链追溯、智能监管、人员培训、应急预案的防控策略。
一、港澳药品入大湾区9市“开闸”,进口审批权下放是关键
2020年11月25日,国家市场监管总局、国家药监局、国家发改委、商务部、国家卫健委、海关总署、国务院港澳办、国家中医药局等八部门联合发布《粤港澳大湾区药品医疗器械监管创新发展工作方案》,该方案聚焦推动大湾区药品医疗器械监管创新,促进区域经济融合发展。方案围绕总体要求、重点任务和保障措施展开。总体要求包括:以习近平新时代中国特色社会主义思想为指导,落实“四个最严”要求,坚持“一国两制”、以人民为中心、分步实施的原则,到2022年建立大湾区内地使用港澳药品医疗器械的体制机制,推动医药产业融合发展,推进中医药国际化;到2035年,完善监管协调机制,实现产业深度融合,建成全国创新发展示范区和国际一流湾区。
重点任务涵盖:药品进口审批改革,允许大湾区内地9市指定医疗机构使用港澳上市药品;加快审评检查分中心建设,建立便捷审评审批机制;简化外用中成药注册审批流程,推进中医药产业发展;开展药品上市许可持有人和医疗器械注册人制度改革;在中山市设立药品进口口岸。
保障措施包括:建立协作机制,健全配套制度,落实监管责任,强化主体责任,完善救济体系。方案通过创新监管方式、整合资源、推动产业发展,为大湾区居民提供优质药品医疗器械和服务,助力健康湾区建设。
二、港澳药品临床急需:全链条风险点与防控策略
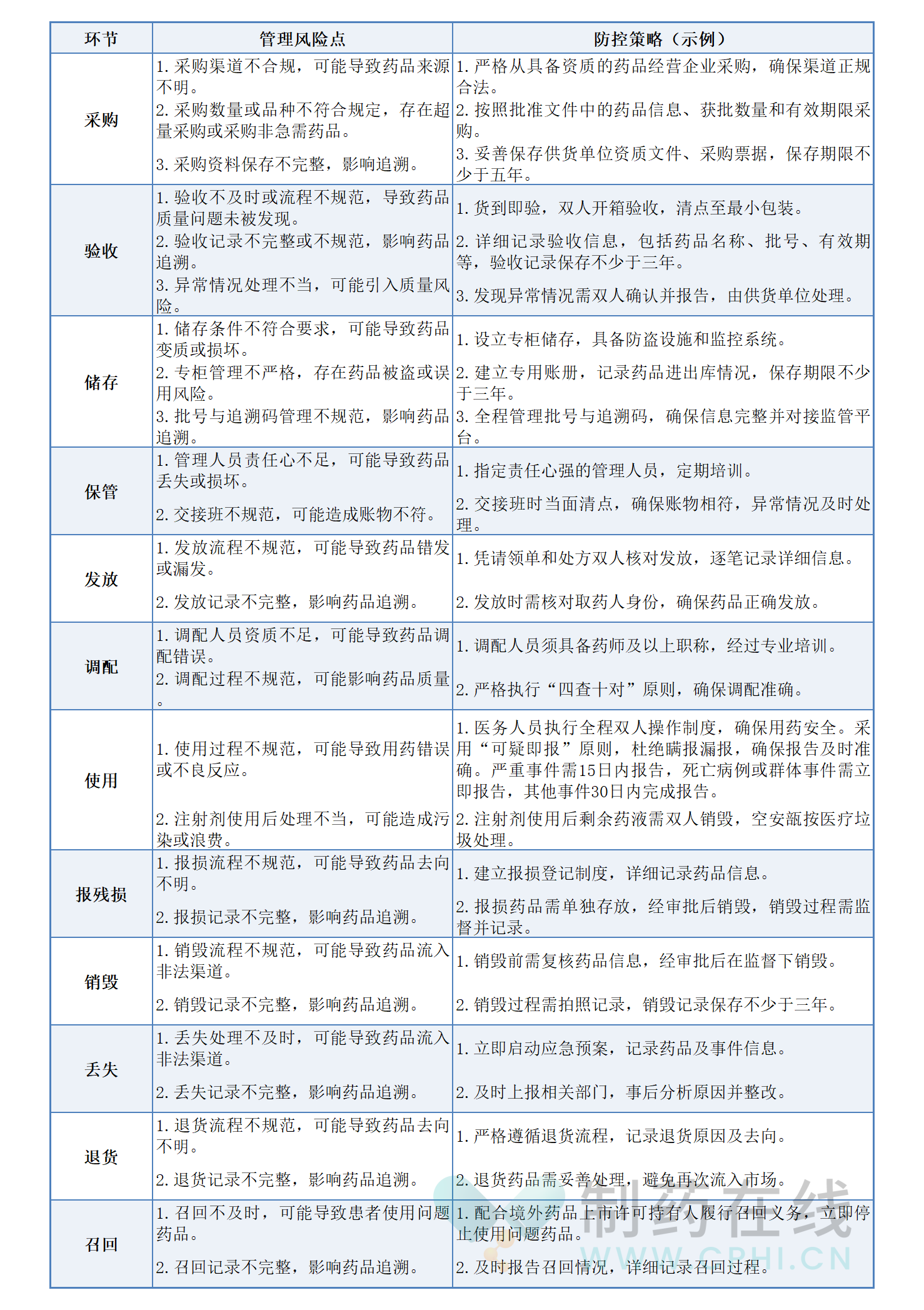
《广东省粤港澳大湾区内地九市进口港澳药品管理专家共识》以法律法规为基础,遵循科学性、规范性与可操作性并重的原则编写。内容全面涵盖临床急需进口港澳药品在指定医疗机构各环节及全流程的管理,具体包括:管理机构与培训考核机制、引进与审核流程、医疗保障管理、采购与供应管理、合理用药指导、处方管理、使用与储存管理、安全管理措施、监督检查机制以及信息化与智能化管理手段等十个方面。以期为医疗机构管理进口港澳药品提供参考。以下是根据《广东省粤港澳大湾区内地九市进口港澳药品管理专家共识》文件内容,对急需港澳药品在采购、验收、储存、保管、发放、调配、使用、报残损、销毁、丢失、退货以及召回等环节的管理风险及干预措施的详细总结表格:
参考文献:
广东省药学会、NMPA等



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57