近日,诺华1类新药「QGE031注射液」在国内获得临床试验默示许可,用于治疗慢性诱导性荨麻疹。

慢性诱导性荨麻疹(CINDU)是一组由特定诱因诱导后出现风团/血管性水肿伴瘙痒的皮肤疾病,其自然病程常常超过6周,发病机制尚不完全清楚。近年来,国内外在CINDU的治疗方面取得一定进展,如传统的抗组胺药、非抗组胺药、生物制剂及小分子靶向药等药物治疗,以及诱因脱敏治疗等物理治疗等。
QGE031(Ligelizumab)是诺华开发的新一代人源化抗IgE单克隆抗体,通过阻断IgE/FcεRI通路发挥作用,被开发用于治疗慢性自发性荨麻疹(CSU)、慢性诱导性荨麻疹(CINDU)、食物过敏等疾病。
2021年1月,QGE031被FDA授予突破性疗法认定,用于治疗对H1 -抗组胺药治疗反应不足的CSU。2021年12月,该药在对H1抗组胺治疗应答不足的慢性自发性荨麻疹(CSU)成人和青少年(≥12岁)患者中开展的2项3期研究(PEARL 1和PEARL 2)取得顶线结果:治疗第12周,QGE031与安慰剂相比在主要终点方面显示出优越性,不过与Xoliris相比没有显示出优越性。
Xolair(omalizumab,奥马珠单抗)是诺华和罗氏旗下基因泰克合作开发的一款抗IgE单克隆抗体,通过降低游离IgE水平,下调高亲和力IgE受体和限制肥大细胞的脱颗粒化,最 大限度地减少过敏性炎症级联反应中多种介导因子的释放。目前,Xolair已在全球获批多个适应症,如中重度持续性过敏性哮喘、慢性特发性荨麻疹和慢性鼻-鼻窦炎伴鼻息肉。
据公司财报,Xolair上市后全球销售额保持稳步增长,2018年至2021年的销售额分别高达29.67亿美元、31.54亿美元、32.81亿美元、35.54亿美元。
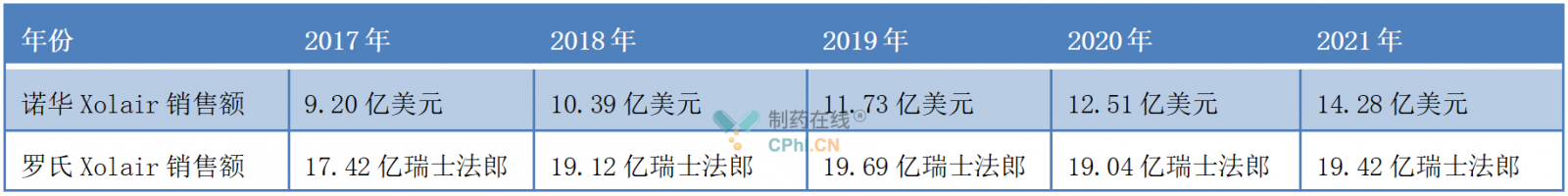
在国内,Xolair于2017年8月被NMPA批准用于治疗12岁以上经吸入激素合并长效β2-肾上腺素受体激动剂治疗控制不佳的中重度过敏性哮喘患者,商品名为茁乐,2019年进入国家医保。
据悉,Xolair的一项关键专利已于2018年年底到期。值得一提的是,去年10月迈博药业在国内递交的CMAB007(奥马珠单抗生物类似药)上市申请获CDE受理。
QGE031作为诺华Xolair的后继产品。据诺华称,QGE031的亲和力大约为Xolair的50倍,两者间对IgE的识别和结合表位存在差异,经亲和力改造的QGE031对IgE/FcεRI信号传导阻滞明显增强。
此外,目前全球还有几款在研抗IgE抗体,如罗氏的Quilizumab、MedImmune的MDI4212。其中Quilizumab是基因泰克开发的第二代抗IgE抗体,靶向细胞膜IgE上的CεmX片段,被开发用于治疗特应性皮炎、过敏性哮喘等疾病。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57