4月5日,基石药业「舒格利单抗注射液」的第5项上市申请获CDE受理。据悉,此次舒格利单抗申报的适应症为:联合化疗一线治疗无法手术切除的局部晚期、复发或转移性食管鳞癌。

舒格利单抗(商品名:择捷美®)是基石药业研发的一款抗PD-L1单抗,据悉其是一种最接近人体的天然G型免疫球蛋白4(IgG4)单抗药物,在患者体内产生免疫原性及相关毒 性的风险更低。
目前,舒格利单抗已在国内获批两项适应症:联合培美曲塞和卡铂用于表皮生长因子受体(EGFR)基因突变阴性和间变性淋巴瘤激酶(ALK)阴性的转移性非鳞状非小细胞肺癌患者的一线治疗,以及联合紫杉醇和卡铂用于转移性鳞状非小细胞肺癌患者的一线治疗(2021/12);用于同步或序贯放化疗后未发生疾病进展的不可切除的III期非小细胞肺癌(NSCLC)患者巩固治疗(2022/05)。
值得一提的是,舒格利单抗已被纳入《2022版CSCO非小细胞肺癌诊疗指南》,推荐联合化疗一线治疗IV期无驱动基因非鳞/鳞状NSCLC患者,以及作为巩固治疗用于同步或序贯放化疗后III期NSCLC患者。
此外,舒格利单抗还先后在国内递交了3项新适应症上市申请,详见下表。
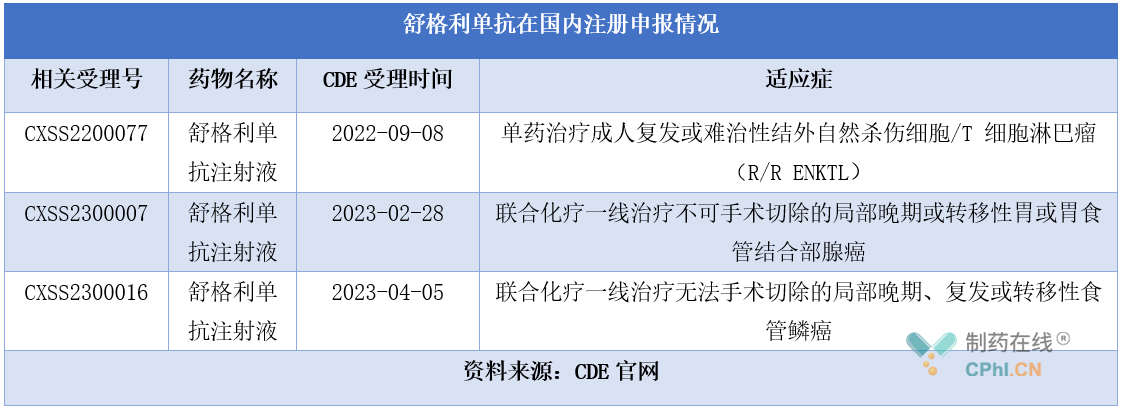
2023年1月,基石药业于宣布舒格利单抗联合化疗一线治疗无法手术切除的局部晚期、复发或转移性食管鳞癌的临床研究GEMSTONE-304达到主要研究终点,显著改善了患者的无进展生存期(PFS)和总生存期(OS)。
食管癌是全球常见的癌症之一。据GLOBOCAN 2020数据,食管癌是全球第8位常见癌症和第6位癌症死亡原因,2020年全球新发病例超过60万例(食管鳞癌约占85%),死亡病例达54.4万例。我国食管癌发病率占全球一半以上,约90%为食管鳞癌,且多数食管鳞癌患者在确诊时已为晚期,失去根治性治疗的机会。GEMSTONE-304研究的成功,使舒格利单抗成为全球首 个针对无法手术切除的局部晚期、复发或转移性食管鳞癌取得阳性结果的PD-L1单抗。
此外,围绕舒格利单抗,基石药业已先后与辉瑞和EQRx公司达成战略合作:2020年9月,基石药业与辉瑞宣布达成总价值为4.8亿美元的战略合作。据协议,辉瑞将以每股约13.37港元的价格购买价值2亿美元的基石药业股份,同时获得舒格利单抗在中国大陆地区的独家商业化权利,而基石药业将获得最高2.8亿美元的里程碑付款以及额外的分级特许权使用费;2020年10月,基石药业将舒格利单抗和抗PD-1单抗CS1003在大中华区以外地区的开发和商业化权益授权给EQRx公司,合作涉及金额高达13亿美元。
目前,在国外,EQRx公司已先后向英国药品和医疗保健用品管理局(MHRA)和欧洲药品管理局(EMA)递交舒格利单抗联合化疗一线治疗转移性NSCLC的上市许可申请。
此外,值得一提的是,在创新药争相降价进入医保的时候,舒格利单抗并未效仿,虽然其获批时间满足医保谈判条件,但基石药业放弃了医保市场,选择进军国际市场。而且,基石药业并未优先选择在美国申报上市,而是选择了英国和欧盟市场,毕竟此前国产PD-1单抗——信迪利单抗和替雷利珠单抗闯关FDA受挫。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57