CD70,又称TNFRSF7,是肿瘤坏死因子(TNF)超家族的成员之一,是一种Ⅱ型跨膜蛋白,与受体CD27作用后可促进T细胞和B细胞活化、增殖及分化,在调控免疫应答过程中发挥重要的作用。
正常情况下,CD70主要表达于活化的淋巴细胞。病理情况下,CD70高表达于多种肿瘤细胞(包括血液恶性肿瘤和实体瘤),可导致免疫功能耗竭,诱导免疫逃逸,与肿瘤的发生发展及预后密切相关,可作为恶性肿瘤早期诊断的新型生物标志物、临床治疗及监测疾病预后的新靶点。
此外,德克萨斯大学MD安德森癌症中心的研究人员发现CD70在EGFR突变的非小细胞肺癌(NSCLC)耐药癌细胞上呈现高度表达,这意味着CD70或将成为一种新的治疗靶点,用于消除常用的EGFR酪氨酸激酶抑制剂(TKI)治疗后仍然存在的耐药癌细胞。
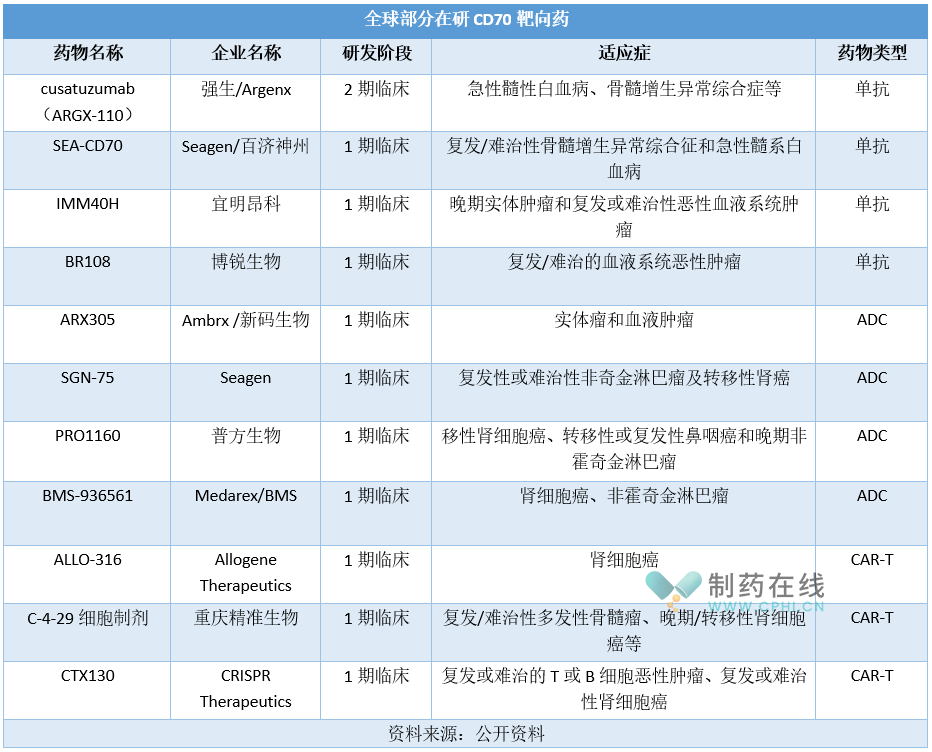
目前,全球已有多家企业布局CD70靶点,详见下表。整体来看,在研CD70靶向药进展较慢,最快的处于2期临床,适应症包括恶性血液肿瘤和实体瘤(尤其是肾细胞癌),药物类型主要为单抗、抗体偶联药物(ADC)和嵌合抗原受体T细胞疗法(CAR-T)。
值得一提的是,我国药企也积极布局CD70靶点。其中宜明昂科、普方生物、博锐生物和重庆精准生物等积极搞自主研发,百济神州、和新码生物依靠"Licensen-in"方式引进CD70靶向药。
• cusatuzumab是Argenx公司基于其强大的美洲驼免疫系统的SIMPLE抗体平台开发的一种CD70靶向单抗,旨在靶向阻断CD70,通过补体依赖性细胞毒 性作用、增强抗体依赖性细胞介导的吞噬作用、增强抗体依赖性细胞介导的细胞毒 性作用,杀死表达CD70的癌细胞,恢复对实体瘤的免疫监测。
在针对初治急性骨髓性白血病(AML)患者的1/2期临床试验中,cusatuzumab与阿扎胞苷(azacitidine)联合使用,与阿扎胞苷单独使用的历史数据相比,有更高的完全缓解率(67%)。2019年ASH年会上公布的cusatuzumab治疗AML和高风险骨髓增生异常综合征(MSD)的1/2期临床试验结果表明:cusatuzumab达到高达92%的总缓解率和42%的完全缓解率。
2018年12月,强生斥资16亿美元获得cusatuzumab的授权。但基于对cusatuzumab现有临床数据的审查,以及对AML护理标准不断发展的考虑,2021年强生终止与argenx公司就cusatuzumab达成的合作许可协议。2023年3月,OncoVerity公司又从argenx公司获得开发cusatuzumab的全球权益,并完成了3000万美元的A轮融资。
• SEA-CD70是Seagen公司开发的一款CD70靶向单抗。2019年11月,百济神州与Seagen公司达成合作协议,获得SEA-CD70在亚洲(除日本)以及其他一些地区的权益。2021年6月,SEA-CD70在国内获批临床,用于治疗复发/难治性MSD和AML。
• IMM40H是一款具有细胞毒作用(ADCC)加强活性的人源化 IgG1 CD70单抗。体内药效研究证明,IMM40H对多种肿瘤具有显著抑瘤活性,较低剂量 2-3 次治疗即可全部清除皮下肿瘤;体外实验研究结果表明,与cusatuzumab analogue相比,IMM40H 具有更强的CD70亲和力,这使其能够更有效地阻断CD70与CD27的相互作用。2022年9月,IMM40H在国内启动1期临床。
• BR108是一款靶向CD70的创新型ADCC增强型单抗。临床前研究表明,BR108与CD70具有很高的亲和力,可通过抗体依赖性细胞介导的ADCC、抗体依赖的细胞介导的吞噬作用(ADCP)、补体依赖的细胞毒 性作用(CDC)杀伤多种CD70阳性肿瘤细胞。此外,BR108还可阻断CD70与其受体CD27的相互作用,解除免疫抑制的肿瘤微环境。在体内药效和毒理研究中,BR108展现了较好的抗肿瘤活性和良好的安全性。2023年1月,BR108在国内获批临床,用于治疗复发/难治性血液系统恶性肿瘤。
• ARX305是一款人源化抗CD70单克隆抗体共价结合2个微管抑制剂AS269而成的ADC。相较于传统ADC药物,ARX305偶联稳定,血液中稳定性高,在多个CD70表达肿瘤模型中显示良好的抑瘤效果;同时,ARX305在动物模型上表现出良好的安全性特征。2019年10月,新码生物与Ambrx达成合作,获得后者ARX305在中国的开发和商业化授权。
• PRO1160是一种ADC,由一种新型的针对CD70的专有抗体通过ProfoundBio专有的ADC平台技术,与exatecan有效载荷偶联组成。PRO1160在实体瘤和淋巴瘤的临床前模型中产生了强大的抗肿瘤作用,同时在大鼠中保持了与亲本mAb相似的PK特征,并在一项非人灵长类动物安全性试验中具有良好的耐受性。
临床前研究数据展示PRO1160具有宽泛的治疗窗口,有望成为同类最 佳ADC疗法的潜力。目前,PRO1160正在进行一项1期临床,旨在评估其在转移性肾细胞癌、转移性或复发性鼻咽癌和晚期非霍奇金淋巴瘤患者中的安全性、活性和药代动力学特点。
• BMS-936561是Medarex/BMS开发的一种CD70靶向ADC,抗体通过蛋白酶敏感型linker与MGBA相连。在临床前研究中,低剂量MDX-1203在PXDX模型中已表现出强有效的抗肿瘤活性,对淋巴瘤和肾细胞癌(RCC)模型疗效良好且毒副作用较低。
• ALLO-316是一款靶向CD70的同种异体CAR-T疗法,由一种靶向CD70的全人源单链抗体、一种基于利妥昔单抗的关闭开关,以及4-1BB和CD3ζ信号域组成。目前,ALLO-316正在进行一项1期TRAVERSE试验,旨在评估ALLO-316在晚期或转移性透明细胞RCC患者中的安全性、耐受性和活性。2022年3月,ALLO-316被FDA授予快速通道资格(FTD),用于治疗晚期或转移性透明细胞肾细胞癌(RCC)患者。
• C-4-29细胞制剂是BCMA/CD70双靶向CAR-T产品,在探索性临床试验中显示具有良好的安全性和有效性,作为靶向多发性骨髓瘤的首 个多靶点产品,有望在临床上进一步降低肿瘤的复发风险。目前,C-4-29细胞制剂已先后在国内获批两项临床试验,适应症为18岁及以上的复发/难治性多发性骨髓瘤和CD70表达阳性的晚期肾细胞癌。
• CTX130是一种健康供体衍生的基因编辑的异体CAR-T研究性疗法,靶向CD70。目前,CTX130正在进行两个独立的1期单臂、多中心、开放标签临床试验,旨在评估CTX130在成年患者中的几个剂量水平的安全性和有效性,COBALT-LYM试验针对复发或难治的T或B细胞恶性肿瘤,COBALT-RCC试验则针对复发或难治性肾细胞癌。2022年9月,CTX130被FDA授予再生医学高级疗法(RMAT)认证,针对皮肤T细胞淋巴瘤(CTCL),真菌病和塞扎里综合征(MF/SS)。
此外,目前已有企业开始研发CD70靶向CAR-NK细胞疗法。2021年5月,CRISPR Therapeutics和Nkarta达成战略合作,共同开发和商业化靶向CD70和未知靶点的两款CAR-NK细胞疗法。
然而,CD70靶向药的开发并不顺利。CD70靶向ADC,如安进的AMG 172和BMS的MDX-1203均已停止,Seagen的ADC药物SGN-75和SGN-CD70也均因毒 性原因停止了临床试验。
总结
免疫疗法是近年来肿瘤药物研发的热门领域。CD70作为免疫治疗潜力靶点,是国内外药企积极布局的热门方向,多款在研药物已显现出治疗恶性血液肿瘤和肾细胞癌等实体瘤的潜力。而且,CD70靶向药药物类型多样,涉及单抗、ADC和CAR-T,我国药企重庆精准生物还研发出了BCMA/CD70双靶向CAR-T疗法。此外,最新研究发现,CD70还有可能成为EGFR突变,并已经发生获得性EGFR TKI耐药性肿瘤的干预靶标之一。然而,CD70靶向药的开发仍充满挑战,AMG 172等多款药物研发停止。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57