近日,药品经营和使用领域掀起了一股不小的波澜。朋友圈和各大行业群聊中,关于随货同行单升级的讨论如火如荼,各种"拒收"的威胁函件满天飞,让药品生产企业质量部和物流部同仁们苦不堪言。甚至一些药品生产厂家也受到了波及,感受到了前所未有的压力。
据了解,此次事件的起因是北京市部分药品经营企业开始要求随货同行单上必须打印销售日期等信息,否则将拒绝接收相关药品。这一要求的提出,立即引发了行业的广泛关注和热议。一方面,支持这一要求的观点认为,打印销售日期等信息可以提高药品的可追溯性,有助于保障药品质量和安全。另一方面,反对的声音也不容忽视。突如其来的要求让他们措手不及,需要投入大量的人力和物力去升级随货同行单,这对于一些小型企业来说无疑是一笔不小的负担。单方面的强硬要求不仅可能引发市场混乱,还可能对供应链的稳定性和药品的正常流通造成影响。
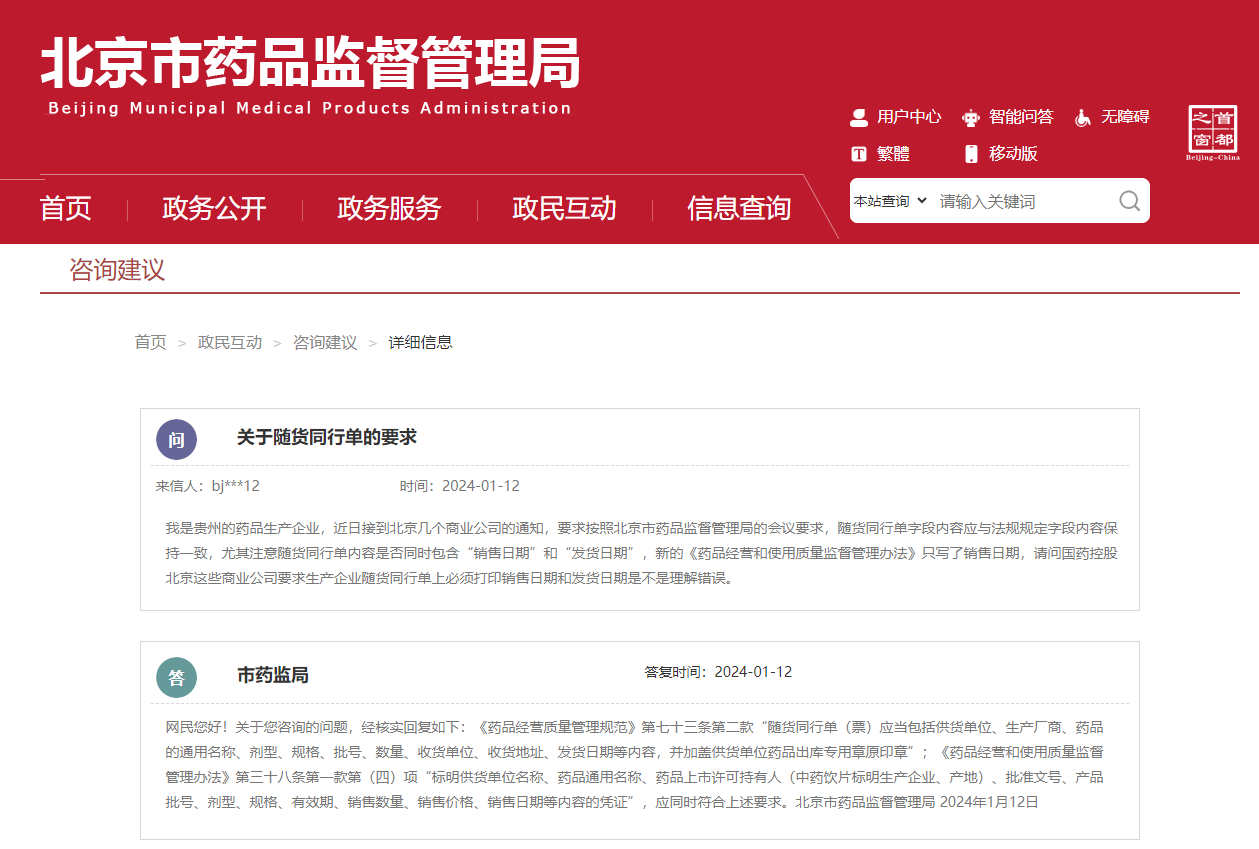
事件仍在持续发酵中。不少药品生产企业已经开始紧急行动起来,在北京市药监局官网留言问询,北京市药监局官方回复:应同时符合《药品经营质量管理规范》和《药品经营和使用质量监督管理办法》的要求,如下图:
一、药品流通新规范:销售与发货日期双重要求,确保药品流通透明与安全
随货同行单上为什么必须明确标注销售日期和发货日期?
这一举措旨在提高药品流通的透明度和可追溯性,确保公众用药安全。销售日期与发货日期虽然有所区别,但同样重要。销售日期通常指的是系统下单日期,即药品在计算机系统中被确认销售的时刻。而发货日期则是药品实际从仓库出库、开始运输的日期。这两个日期虽然不一定相同,但都对于药品流通的监管至关重要。
通过明确标注销售日期,可以追溯药品的销售记录和市场需求情况,有助于规范市场秩序和防止非法销售行为。而发货日期的标注,则能够准确反映药品的运输时效和到货时间,保障药品的及时送达和患者用药的及时性。
为了确保这一新规范的顺利实施,供应商和药品经营企业需要积极配合,升级随货同行单系统,确保能够准确、清晰地打印出销售日期和发货日期。同时,相关监管部门也应加大监督和检查力度,确保药品流通领域的规范有序。
总之,销售日期和发货日期的双重要求是药品流通领域规范化管理的重要举措之一。通过这一措施的实施,将有助于提高药品流通的透明度和可追溯性,保障公众用药安全。
二、关于药品购销记录/随货同行单的法规要求
随着药品监管政策的日益严格,自1月1日起,全国范围内的药品流通领域将迎来一场重要的变革。据权威部门发布,届时若药品随货同行单未能完成升级,相关药品将被严格"拒收",此举旨在提高药品流通的透明度和可追溯性,保障公众用药安全,笔者梳理了一下关于药品购销记录/随货同行单的法规要求,如下表:
|
法规 |
法规要求摘要 |
|
《中华人民共和国药品管理法》 |
第五十七条药品经营企业购销药品,应当有真实、完整的购销记录。购销记录应当注明药品的通用名称、剂型、规格、产品批号、有效期、上市许可持有人、生产企业、购销单位、购销数量、购销价格、购销日期及国务院药品监督管理部门规定的其他内容。 |
|
2024年1月1日实施的《药品经营和使用质量监督管理办法》 |
第三十八条药品上市许可持有人、药品批发企业销售药品时,应当向购药单位提供以下材料:(四)标明供货单位名称、药品通用名称、药品上市许可持有人(中药饮片标明生产企业、产地)、批准文号、产品批号、剂型、规格、有效期、销售数量、销售价格、销售日期等内容的凭证; |
|
第五十三条医疗机构应当建立和执行药品购进验收制度,购进药品应当逐批验收,并建立真实、完整的记录。 药品购进验收记录应当注明药品的通用名称、药品上市许可持有人(中药饮片标明生产企业、产地)、批准文号、产品批号、剂型、规格、有效期、供货单位、购进数量、购进价格、购进日期。 |
|
|
2016年7月13日发布实施的《药品经营质量管理规范》(国家食品药品监督管理总局令(2016年)第28号) |
第七十三条第二款“随货同行单(票)应当包括供货单位、生产厂商、药品的通用名称、剂型、规格、批号、数量、收货单位、收货地址、发货日期等内容,并加盖供货单位药品出库专用章原印章”; |
|
2009年6月2日国家食品药品监督管理局发布的《关于规范药品购销活动中票据管理有关问题的通知》(国食药监安[2009]283号) |
各级食品药品监督管理部门要加强对药品购销活动中票据管理的监管工作,督促药品生产、经营企业按照以下要求从事药品购销活动:所销售药品还应附销售出库单,包括通用名称、剂型、规格、批号、有效期、生产厂商、购货单位、出库数量、销售日期、出库日期和销售金额等内容,税票(包括清单,下同)与销售出库单的相关内容应对应,金额应相符。 |
|
重庆、四川《药品批发企业检查细则》 |
1003随货同行单(票)应当包括供货单位、药品上市许可持有人、生产企业、药品的通用名称、剂型、规格、批号、有效期、数量、收货单位、收货地址、发货日期等。 1.企业留存的随货同行单(票),内容应当完整,具有供货单位出库专用章。其收货单位、收货地址与企业情况应当相符。 *1307药品出库时,应加盖药品出库专用章的随货同行单。 1.企业应当明确随货同行单(票)应载明的内容,包括:企业名称、药品上市许可持有人、生产企业、药品的通用名称、剂型、规格、批号、数量、购货单位、收货地址、发货日期等; 2.企业药品出库时应当附随货同行单(票),随货同行单(票)应当加盖药品出库专用章。 |
|
2016年12月16日,原CFDA官网发布《药品经营质量管理规范现场检查指导原则(修订稿)》 |
06801采购药品应当建立采购记录,包括药品的通用名称、剂型、规格、生产厂商、供货单位、数量、价格、购货日期等内容,采购中药材、中药饮片的还应当标明产地等。09201企业应当做好药品销售记录,应当包括药品的通用名称、规格、剂型、批号、有效期、生产厂商、购货单位、销售数量、单价、金额、销售日期等内容。 07302随货同行单(票)应当包括供货单位、生产厂商、药品的通用名称、剂型、规格、批号、数量、收货单位、收货地址、发货日期等内容,并加盖供货单位药品出库专用章原印章。 |
|
药品经营质量管理规范现场检查指南.批发篇/国家药品监督管理局高级研修学院组织编写.-2版.一北京:中国人口出版社,2018.12 |
检查企业随货同行单(票),核实其内容是否符合07302(随货同行单(票)应当包括供货单位、生产厂商、药品的通用名称、剂型、规格、批号、数量、收货单位、收货地址、发货日期等内容,并加盖供货单位药品出库专用章原印章)检查项目的要求。 |
|
2016年12月26日原食品药品监管总局发布 附录4《药品收货与验收》(2016年第197号) |
第三条药品到货时,收货人员应当查验随货同行单(票)以及相关的药品采购记录。无随货同行单(票)或无采购记录的应当拒收;随货同行单(票)记载的供货单位、生产厂商、药品的通用名称、剂型、规格、批号、数量、收货单位、收货地址、发货日期等内容,与采购记录以及本企业实际情况不符的,应当拒收,并通知采购部门处理。 |
|
第四条应当依据随货同行单(票)核对药品实物。随货同行单(票)中记载的药品的通用名称、剂型、规格、批号、数量、生产厂商等内容,与药品实物不符的,应当拒收,并通知采购部门进行处理。 |
|
|
2016年12月26日原食品药品监管总局发布 附录1《冷藏、冷冻药品的储存与运输管理》(2016年第197号) |
第四条企业应当按照《规范》的要求,对冷藏、冷冻药品进行收货检查。 (一)检查运输药品的冷藏车或冷藏箱、保温箱是否符合规定,对未按规定运输的,应当拒收。 (二)查看冷藏车或冷藏箱、保温箱到货时温度数据,导出、保存并查验运输过程的温度记录,确认运输全过程温度状况是否符合规定。 (三)符合规定的,将药品放置在符合温度要求的待验区域待验;不符合规定的应当拒收,将药品隔离存放于符合温度要求的环境中,并报质量管理部门处理。 (四)收货须做好记录,内容包括:药品名称、数量、生产企业、发货单位、运输单位、发运地点、启运时间、运输工具、到货时间、到货温度、收货人员等。 |
参考文献
[1] NMPA、北京药监局等



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57