PD-(L)1单抗是肿瘤免疫治疗领域取得巨大成功的一类药物。而TGF-β通过刺激肿瘤微环境的上皮间质转化、血管生成、癌症相关成纤维细胞激活和免疫抑制来促进肿瘤进展,与PD-(L)1 抗体耐药产生有关。理论上,开发PD-(L)1/TGF-β双靶点疗法能够同时阻断TGF-β介导的下游肿瘤激活通路以及PD-1介导的肿瘤免疫逃逸作用来实现双重的抗肿瘤活性。
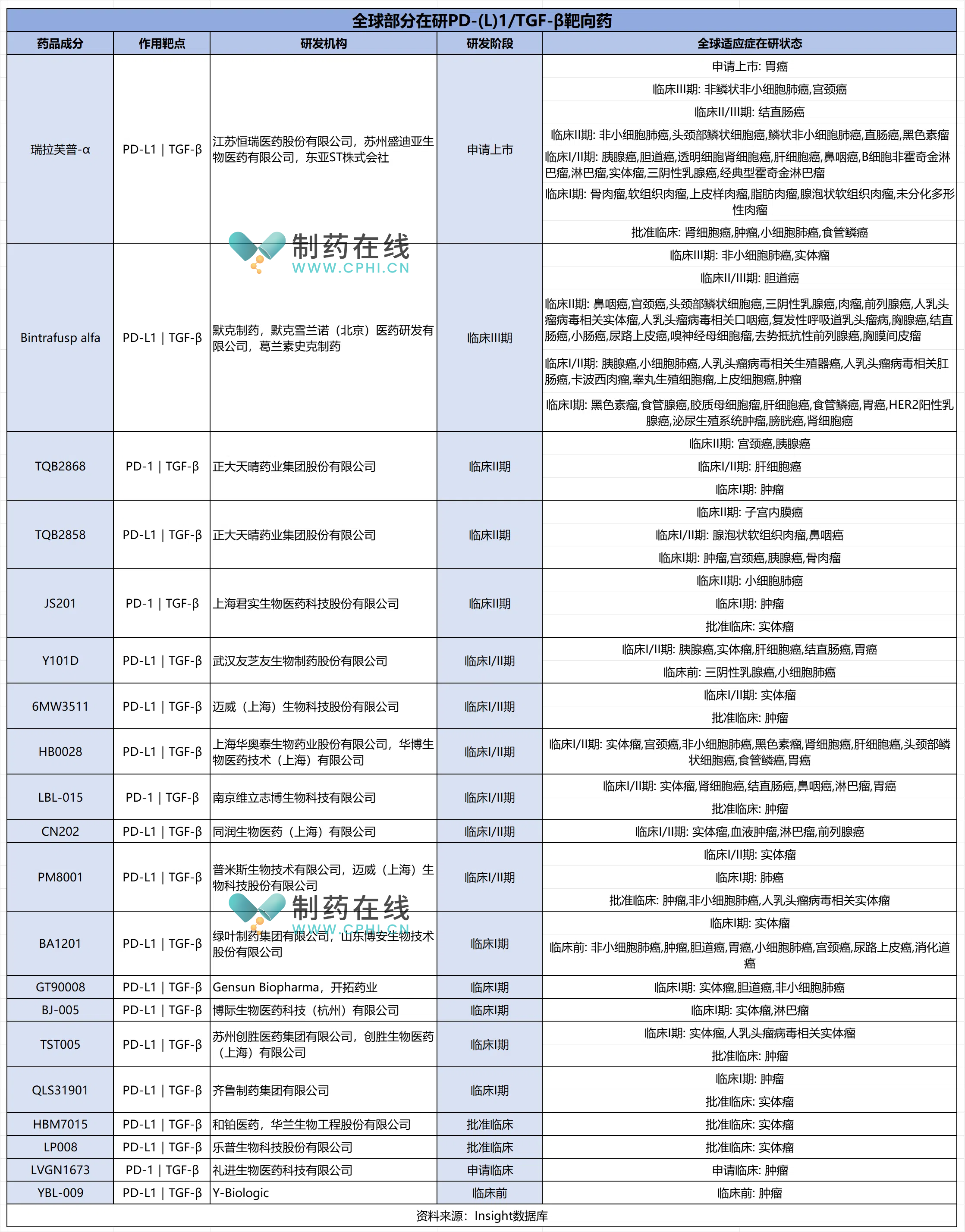
据Insight数据库,目前全球药企已开发出多款在研PD-(L)1/TGF-β双靶向药物,详见下表。从布局企业看,我国药企在PD-(L)1/TGF-β领域布局广泛,活跃的产品管线较多。适应症上,在研药物主要被开发用于治疗胃癌、宫颈癌、肺癌等实体瘤。研发进度上,在研药物大多处于I、II期临床,默克的Bintrafusp alfa处于第二梯队,已进入III期临床。恒瑞医药的瑞拉芙普-α进展最快,已经申请上市。
瑞拉芙普-α(SHR-1701)是恒瑞医药自主研发并具有知识产权的抗PD-L1/TGF-βRII双功能融合蛋白,由抗PD-L1抗体重链的C末端氨基酸通过接头蛋白片段(G4S)4G连接TGF-βRⅡ胞外区的N末端氨基酸而成,其可以促进效应性T细胞的活化,还可有效改善肿瘤微环境中的免疫调节作用,最终有效促进免疫系统对于肿瘤细胞的杀伤。在剂量递增、剂量扩展和临床扩展的1期研究中,SHR-1701单药治疗在重度预处理的胃癌队列中显示出良好的抗肿瘤活性。
ESMO 2024大会上公布的SHR-1701联合化疗对比安慰剂联合化疗一线治疗HER2阴性胃或胃食管结合部腺癌(G/GEJA)的III期临床研究结果表明:SHR-1701联合化疗组在主要研究终点上显著优于安慰剂联合化疗组,可显著延长G/GEJA患者的总生存期,且未发现新的安全性风险信号,安全性可接受。
具体数据为:在PD-L1 CPS≥5人群中,SHR-1701组和安慰剂组的中位生存期(mOS)分别为16.8个月和10.4个月,达到统计学差异;在ITT人群中,SHR-1701组和安慰剂组mOS分别为15.8个月和11.2个月,达到统计学差异;在PD-L1 CPS≥5人群中,SHR-1701组和安慰剂组的中位无进展生存期(mPFS)分别为7.6个月和5.5个月,ORR分别为56.5%和32.7%,DoR分别为10.2个月和5.1个月;在ITT人群中,SHR-1701组和安慰剂组的mPFS分别为7.0个月和5.5个月,ORR分别为53.4%和32.8%,DoR分别为8.5个月和5.3个月。
安全性方面,贫血、血小板减少、呕吐是治疗中较常见的不良反应。SHR-1701联合CAPOX治疗组患者和安慰剂联合CAPOX治疗组患者的总体TRAE相似,分别是97.8%和98.4%。其中≥3级TRAE分别为62.6%和59%,严重TRAE分别为34.9%和24%。未发现新的安全性信号。
2024年9月,瑞拉芙普-α在国内申请上市,具体适应症为:联合氟尿嘧啶类和铂类药物用于局部晚期不可切除、复发或转移性胃及胃食管结合部腺癌的一线治疗。
此外,SHR-1701还被开发用于治疗肺癌、直肠癌、鼻咽癌等肿瘤。其中SHR-1701联合或不联合化疗新辅助治疗不可切除的Ⅲ期非小细胞肺癌的概念验证II期临床研究(TRAILBLAZE研究)成果于2024年6月在《Cancer Cell》期刊上发表,结果显示:在接受新辅助联合治疗的主要队列患者(n=97)中,两项主要终点均达到,诱导后的ORR为58% ,18个月无事件生存率(EFS)为56.6%。27例(25%)患者接受了手术治疗,均达到R0切除,其中主要病理缓解(MPR)为44%,完全病理缓解(pCR)为26%;手术治疗组18个月EFS率为74.1% ,放疗组18个月EFS率为57.3%。
SHR-1701联合氟唑帕利维持治疗晚期肺鳞状细胞癌(LUSC)的单臂II期临床试验亮相2024世界肺癌大会(WCLC),结果显示:SHR-1701联合氟唑帕利维持治疗晚期肺鳞癌患者展现出令人鼓舞的临床活性和可控的安全性。
SHR-1701是全球首个申请上市的PD-(L)1/TGF-β双靶向药物,2020年11月,恒瑞医药以1.3927亿美元交易总额将SHR-1701在韩国的独家临床开发、生产和市场销售的权利许可给韩国DONG-AST公司。
Bintrafusp alfa是一种双功能融合蛋白,由抗PD-L1融合到人类TGF-β受体Ⅱ的胞外域组成,在先前的一项I期和单中心II期试验中,接受Bintrafusp Alfa治疗的HPV相关肿瘤(包括宫颈癌)患者的总临床缓解率为30.0%。
临床前模型表明,TGF-β信号转导可促进宫颈癌的上皮-间充质转化、血管生成和纤维化,从而导致对抗癌疗法(包括免疫疗法)的耐药性和较差的生存结局。因此同时抑制TGF-β和PD-L1两种免疫抑制通路可能会改善宫颈癌患者的预后。
值得一提的是,Bintrafusp Alfa治疗复发性或转移性宫颈癌的一线II期临床研究荣登2024年7月的JAMA Oncology期刊。研究结果显示:Bintrafusp Alfa在既往接受过铂类化疗失败的复发性或转移性宫颈癌患者中证明了其临床活性,达到了研究的主要终点,IRC评估的cORR为21.9%,鳞状细胞癌和HPV阳性亚组的ORR更高。
总结
整体来看,国内外药企积极布局PD-(L)1/TGF-β靶向药,且国内药企居多。但在研PD-(L)1/TGF-β靶向药2024年至今取得新进展的较少。恒瑞医药瑞拉芙普-α的申请上市,不仅给复发或转移性胃及胃食管结合部腺癌的一线治疗提供新选择,也给PD-(L)1/TGF-β靶向药布局企业以信心。此外,默克的Bintrafusp Alfa在治疗复发性或转移性宫颈癌方面也表现积极。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57