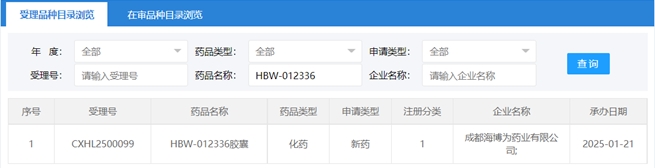
1月21日,成都海博为药业有限公司1类新药「HBW-012336胶囊」的临床试验申请获CDE受理。据公开资料,HBW-012336是一款口服KRAS G12D抑制剂,拟用于治疗多种携带KRAS G12D突变的肿瘤。
HBW-012336具有治疗携带KRAS G12D突变肿瘤的潜力。在多种小鼠移植瘤模型中,HBW-012336表现出显著的抗肿瘤药效,且同等剂量下抑瘤效果显著优于处于1期临床的非共价、强效、选择性KRAS G12D抑制剂MRTX1133。而且,HBW-012336在人结肠癌细胞LS513异种移植模型中与西妥昔单抗联用有明显的协同增效作用。
此外,HBW-012336安全性高。临床前研究显示其对心血管、呼吸系统和中枢神经系统无明显影响,无基因毒性,单药和重复给药的毒理研究中均表现出足够的安全性。
KRAS G12D抑制剂进展
KRAS是实体瘤中的主要原癌基因之一,据统计约1/7的肿瘤患者携带KRAS基因的突变,且KRAS突变在不同肿瘤中的发生率不同,其中约90%的胰腺癌、40%的结直肠癌和30%的非小细胞肺癌携带该突变。
KRAS G12D突变是KRAS突变中最常见的类型,约占整个KRAS突变的35%,在大约34%的胰腺导管腺癌、12%的结直肠癌和4%的非小细胞肺癌以及其它多种类型癌症中可检测出。而且,有显著证据表明与其他KRAS突变相比,G12D突变赋予更强的免疫抑制肿瘤微环境和更高的免疫治疗耐药性。
目前,全球尚无KRAS G12D抑制剂获批,但已出现多款在研KRAS G12D抑制剂,详见下表。在研KRAS G12D抑制剂除了小分子化药,还包括蛋白降解剂。研发进度上,KRAS G12D抑制剂较KRAS G12C抑制剂进展慢,大多处于1、2期临床。
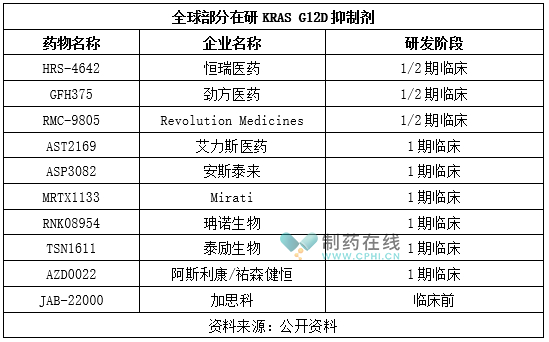
具体品种来看,HRS-4642、GFH375、RMC-9805处于1/2期临床。其中HRS-4642是恒瑞医药研发的一款高效、长效、特异性KRAS G12D抑制剂,其能够特异性结合KRAS G12D,进而抑制MEK和ERK蛋白的磷酸化,从而发挥抗肿瘤作用。研究显示,HRS-4642对KRAS G12D的亲和力是结合KRAS G12C的21倍、野生型KRAS蛋白的17倍。在胰腺癌、结直肠癌、肺腺癌的模型中,HRS-4642展现出符合预期的良好抑制效应,能够有效抑制细胞增殖和肿瘤生长。
2022年8月,HRS-4642在国内获批临床,成为国内首个获批临床的KRAS G12D抑制剂。2023 ESMO大会上公布的1期临床数据显示:入组的18例携带KRAS G12D突变晚期实体瘤患者中13例有基线靶病变的患者至少进行了一次基线后评估,其中1名非小细胞肺癌(NSCLC)患者在接受200mg治疗后出现部分缓解(PR),11名患者出现病情稳定(SD),6名患者出现靶病变缩小,包括肺癌和结直肠癌。而且,HRS-4642暴露量与半衰期约为40小时的剂量大致成比例。
HRS-4642表现出可耐受的安全性,研究中未观察到剂量限制性毒性(DLT),MTD未达到。9例患者观察到3级以上不良事件(AE),6例出现3级以上治疗相关AE。
GFH375 (VS-7375)是劲方医药开发的口服、高选择性KRAS G12D抑制剂,能同时靶向激活(ON)和非激活(OFF)状态的KRAS G12D突变蛋白,在体外实验中显示出对KRAS G12D突变细胞的高效抑制作用,且有很高的选择性。
临床前研究显示:GFH375单药治疗能够显著抑制肿瘤生长,且在动物模型中观察到剂量依赖性的肿瘤消退;GFH375具有治疗KRAS G12D突变型肿瘤脑转移患者的潜力,在颅内肿瘤模型中表显示出显著的抗肿瘤活性;GFH375联合RAF/MEK抑制剂avutometinib在动物模型中显示出协同增效的作用。而且,GFH375在临床前研究中显示出良好的安全性,并且在激酶选择性和安全性靶点测试中具有低脱靶风险。
RMC-9805是一款潜在首 创选择性、共价、口服KRAS G12D抑制剂。已公布的1/1b期临床研究RMC-9805-001(NCT06040541)结果显示:RMC-9805在KRAS G12D突变胰腺导管腺癌(PDAC)中的客观缓解率(ORR)为30%,疾病控制率(DCR)为80%。而且,RMC-9805显示出良好的安全性,且在不同剂量水平上普遍展现良好的耐受性。
AST2169、ASP3082、MRTX1133等处于1期临床。其中AST2169是艾力斯公司自主研发的一款针对KRAS G12D突变的选择性抑制剂,其采用脂质体作为药物载体。2024年3月,该药在国内获批临床,用于治疗携带KRAS G12D突变的晚期实体瘤。
ASP3082是全球首个进入临床阶段的KRAS G12D蛋白降解药物,其通过募集E3泛素连接酶蛋白,与KRAS G12D突变蛋白结合,并选择性地靶向及降解突变的KRAS G12D。
2023年AACR上公布的临床前研究结果显示:ASP3082具有显著的抗肿瘤作用,可选择性地降解KRAS G12D突变蛋白,并抑制KRAS G12D突变癌细胞的生长活性,但在KRAS野生型癌细胞中无此活性。2024年6月,ASP3082在国内获批临床,用于治疗携带KRAS G12D突变的既往经治局部晚期(不可切除)或转移性恶性实体瘤。
TSN1611是泰励生物自主研发的一种靶向携带KRAS G12D突变肿瘤的高效高选择性小分子药物,分别于2024年2月和2024年4月在美国和中国获批临床试验。TSN1611具有良好的理化性质、口服药代动力学特征和显著的脑渗透潜力,其在多种动物模型中表现出卓越的体内抗肿瘤活性和持久的反应。在人类结直肠癌细胞系模型(GP2D模型)和胰腺腺癌上皮细胞系模型(HPAC模型)中,TSN1611显示出剂量依赖性的抗肿瘤功效。
AZD0022是阿斯利康于2023年11月从祐森健恒引进的一款小分子KRAS G12D抑制剂,具有良好的活性和口服生物利用度。2024年10月,AZD0022在美国启动1期临床(ALAFOSS-01),旨在评估其作为单一疗法或与抗癌药物联合治疗KRAS G12D突变成人肿瘤患者的安全性、耐受性、药代动力学和疗效。2025年1月,该药在国内获批临床,用于治疗携带KRAS G12D突变的晚期实体瘤。
总结
整体来看,KRAS G12D抑制剂的开发还有很长的路要走,但已有多款药物取得积极进展。我国药企也积极开发KRAS G12D抑制剂,且在该领域的进度并不落后于国外。期待在药企的不懈努力下,KRAS G12D抑制剂早日迎来重大突破。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57