11月9日,据CDE官网,礼来RET抑制剂「selpercatinib胶囊」的上市申请获受理。
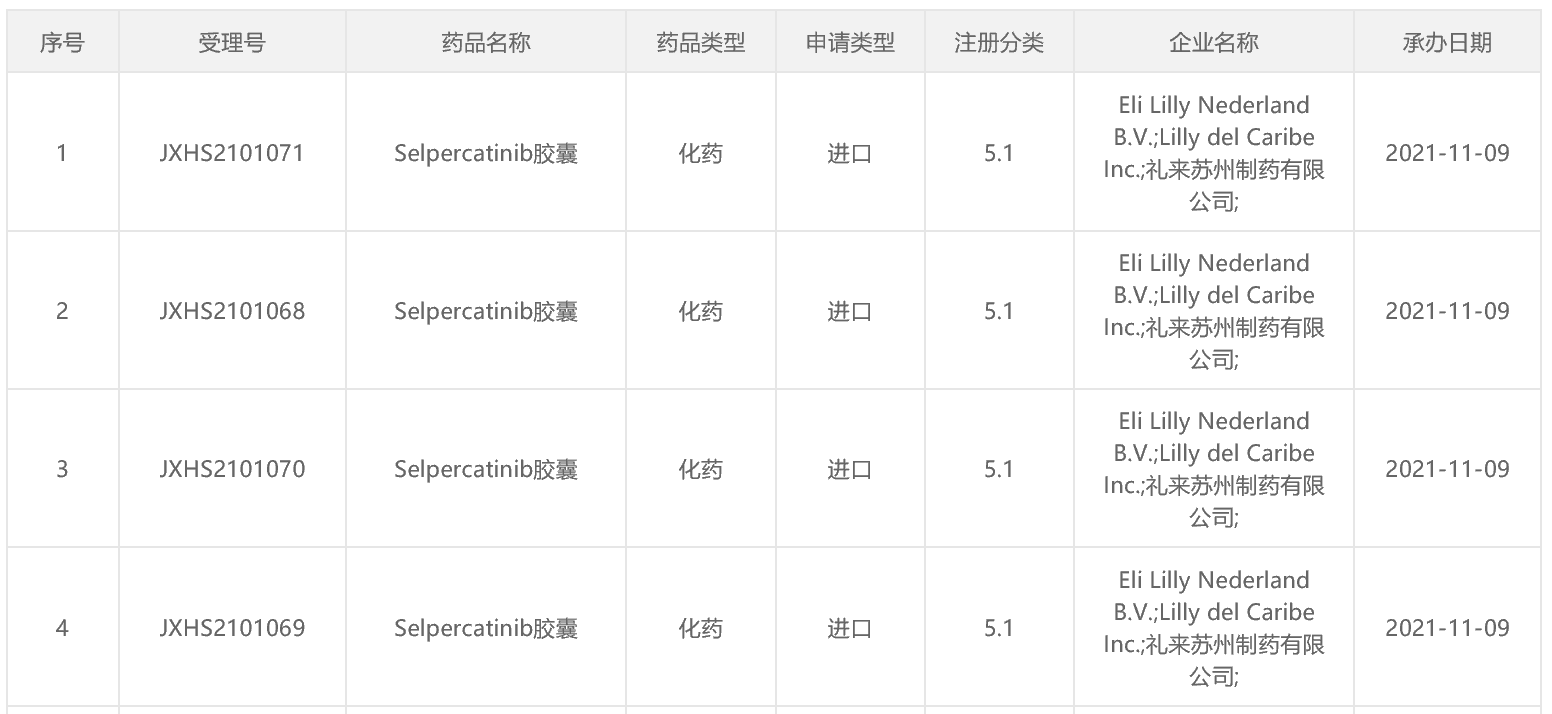
此前该药已被CDE纳入优先审批程序,拟定适应症为:(1)转染重排(RET)基因融合阳性的局部晚期或转移性非小细胞肺癌(NSCLC);(2)RET突变的需要系统性治疗的晚期或转移性甲状腺髓样癌(MTC)成人和12岁及以上儿童患者,以及RET基因融合阳性的需要系统性治疗和**碘治疗(如适用)难治的晚期或转移性甲状腺癌成人和12岁及以上儿童患者。


selpercatinib(LOXO-292)是一款口服、强效、高选择性转染期间重排(RET)激酶抑制剂,旨在抑制天然的RET信号转导以及预期的获得性耐药机制。该药由Loxo Oncology公司开发,2018年先后被FDA授予治疗三类患者的突破性药物资格:(1)接受含铂化疗以及一种PD-1或PD-L1肿瘤免疫疗法治疗后病情进展、需要系统治疗(全身治疗)的转移性RET融合阳性NSCLC患者;(2)既往接受治疗后病情进展且没有可接受的替代治疗选择、需要系统治疗的RET突变型甲状腺髓样癌(MTC)患者;(3)既往接受其他方案后病情进展且没有可接受的替代治疗方案、需要系统治疗的晚期RET融合阳性甲状腺癌患者。
此外,selpercatinib还于2019年被FDA授予孤儿药资格,用于治疗:RET融合阳性NSCLC、RET融合阳性和RET突变甲状腺癌,包括低分化甲状腺癌、未分化或间变性甲状腺癌、MTC、局部晚期或转移性滤泡或乳头状甲状腺癌。
2019年1月,礼来与Loxo Oncology达成最终协议,以每股235美元(约80亿美元)现金收购Loxo Oncology,获得包括selpercatinib在内的多款药物。
2020年5月,selpercatinib被FDA批准用于治疗RET融合阳性的转移性NSCLC成年患者,和需要系统性治疗的携带RET突变的晚期或转移性甲状腺髓样癌成人和12岁及以上的儿童患者,以及需要系统性治疗和**碘治疗(如适用)难治的RET融合阳性的晚期或转移性甲状腺癌成人和12岁及以上的儿童患者,商品名为Retevmo。据公司财报,该药2020年销售额达36.6百万美元,2021上半年销售额达42.5百万美元。
在国内,selpercatinib(LOXO-292)共登记了3项临床试验,详见下图。根据临床试验进度,笔者推测此次selpercatinib的上市申请是基于国外临床试验数据。
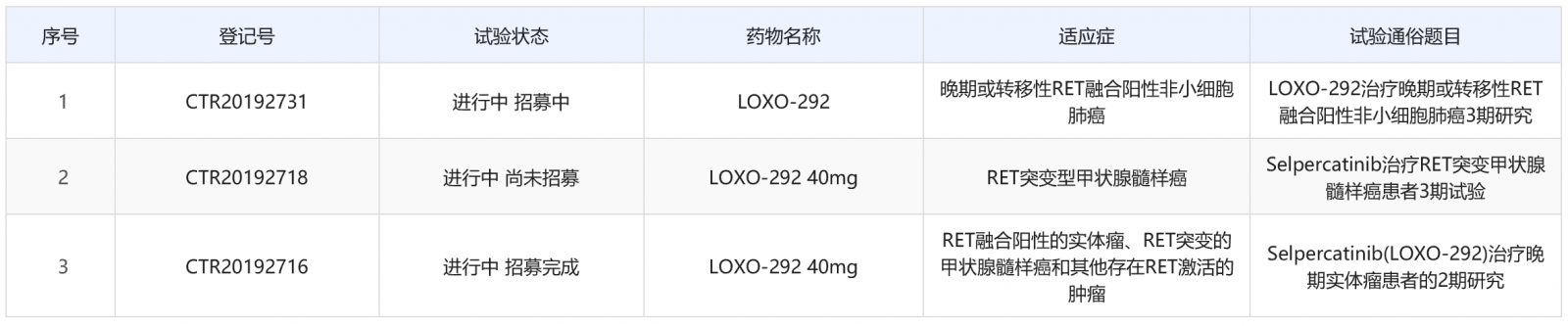
selpercatinib在美国获批是基于I/II期临床研究LIBRETTO-001的数据。该研究是针对RET驱动型癌症患者规模最 大的一项临床试验(N=702),既纳入了初治患者,也纳入了经治的各种晚期实体肿瘤患者,包括RET融合阳性的NSCLC、RET突变的MTC、RET融合阳性的甲状腺癌以及其它RET改变的实体肿瘤。主要疗效结果为由独立评估委员会评估的ORR和DoR。
2020年8月在《新英格兰医学杂志》(NEJM)发表的研究数据显示:(1)针对RET基因融合阳性NSCLC:在未经治疗的患者中,85%的患者达到部分缓解,10%的患者疾病稳定,治疗6个月时,仍有90%的患者对疗法有持续响应。在既往接受过治疗的患者中:2%的患者出现完全缓解,62%的患者部分缓解,29%的患者疾病稳定;中位持续缓解时间为17.5个月,在中位随访时间12个月时,有63%的患者仍然处于缓解状态;中位无进展生存期(PFS)为16.5个月。(2)针对RET突变髓样甲状腺癌:在55名此前接受过治疗的RET突变髓样甲状腺癌患者中,客观缓解率为69%,一年无进展生存率为82%;在88名此前未接受治疗的RET突变髓样甲状腺癌患者中,客观缓解率为73%,一年无进展生存率为92%;(3)在19名接受过治疗的RET融合甲状腺癌患者中,客观缓解率为79%,一年无进展生存率为64%。
RET基因位于10号染色体的长臂上,编码一个受体酪氨酸激酶,在正常神经元、交感神经和副交感神经节、甲状腺C细胞、肾上腺髓细胞、泌尿生殖道细胞、睾丸生殖细胞都有表达。其蛋白活化后会激活下游的信号通路(包含RAS、MAPK、ERK、PI3K、AKT等),导致细胞增殖、迁移和分化。
RET基因突变包括融合和点突变,发生在多种肿瘤中,但不同肿瘤中,RET突变的发生率不同。据统计,大约1%-2% NSCLC患者发生RET基因融合,超过60%的MTC患者发生RET基因点突变,10%的乳头状甲状腺癌患者发生RET基因融合。
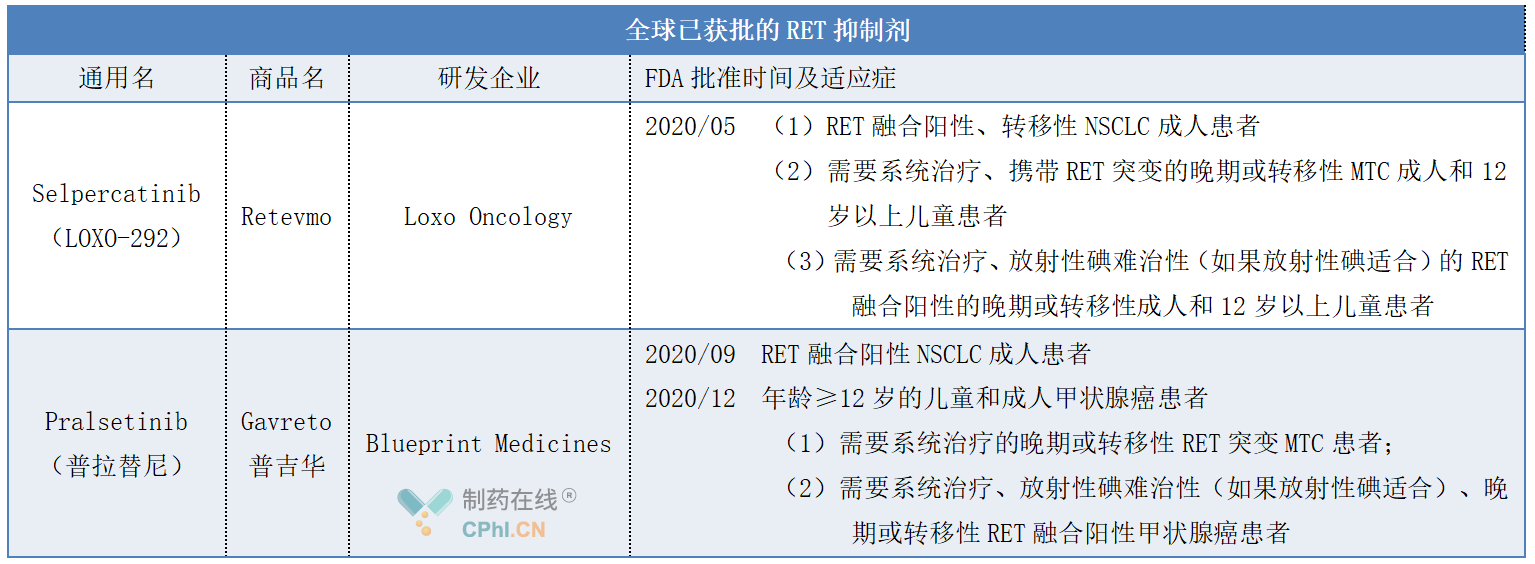
目前,全球已经批准2款RET抑制剂(详见下表),其中Gavreto被基石药业引进国内,已于今年3月在国内被批准用于既往接受过含铂化疗的RET融合阳性的局部晚期或转移性NSCLC患者。此次selpercatinib在国内递交上市申请,有望成为国内获批的第二款RET抑制剂。
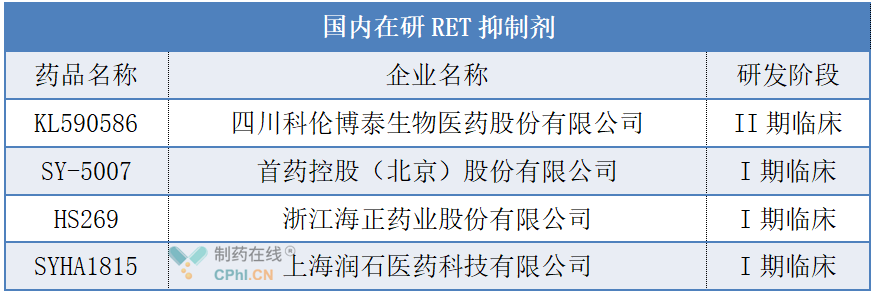
此外,目前我国还有多款在研RET抑制剂,详见下表。其中科伦博泰自主研发的KL590586进展较快,被开发用于治疗RET融合或突变的晚期实体瘤。临床前研究显示:KL590586对RET激酶具有高选择性,在动物模型中显示出良好的抗肿瘤活性和安全性;与全球已上市的同类药相比,在动物血/脑暴露量方面具有优势,且对已有报道的多种临床耐药突变有效,具有治疗肿瘤脑转移和克服临床耐药突变的潜力。今年3月,科伦博泰将该药在欧美等区域权利有偿独家授权给Ellipses。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57