2021年11月16日,国家住房和城乡建设部办公厅官网发布了《医药工业洁净厂房施工与验收标准(征求意见稿)》,征求意见反馈截止时间为2021年12月12日。该标准为首次制定,由中国医药工程设计协会牵头起草,中石化上海工程有限公司等单位起草,对于医药企业厂房的建设具有重要指导意义。为医药工业洁净厂房相关方提供了具有可操作性的医药工业洁净厂房施工与验收相关标准。
一、《医药工业洁净厂房施工与验收标准》标准信息

二、《医药工业洁净厂房施工与验收标准》有哪些关注点?
1.适用范围关注点

2.医药工业洁净厂房施工验收关注点
2.1 洁净厂房施工验收类型和检测状态
医药工业洁净厂房施工验收,参考GB51110-2015《洁净厂房施工及质量验收规范》可分为竣工验收、功能验收、使用验收三种类型,验收的检测状态可分为空态、静态和动态。

2.2 医药工业洁净厂房验收测试项目
医药洁净区各项性能检测前,净化空调系统应正常运行24小时以上,并应达到稳定运行状态,根据不同洁净区级别,医药洁净区的验收的测试项目详见下表:
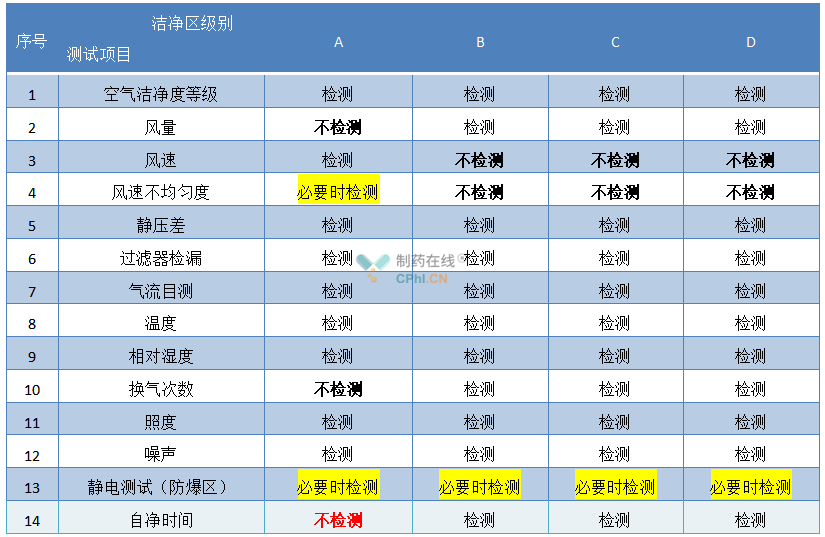
2.3 医药工业洁净厂房特殊施工验收项目
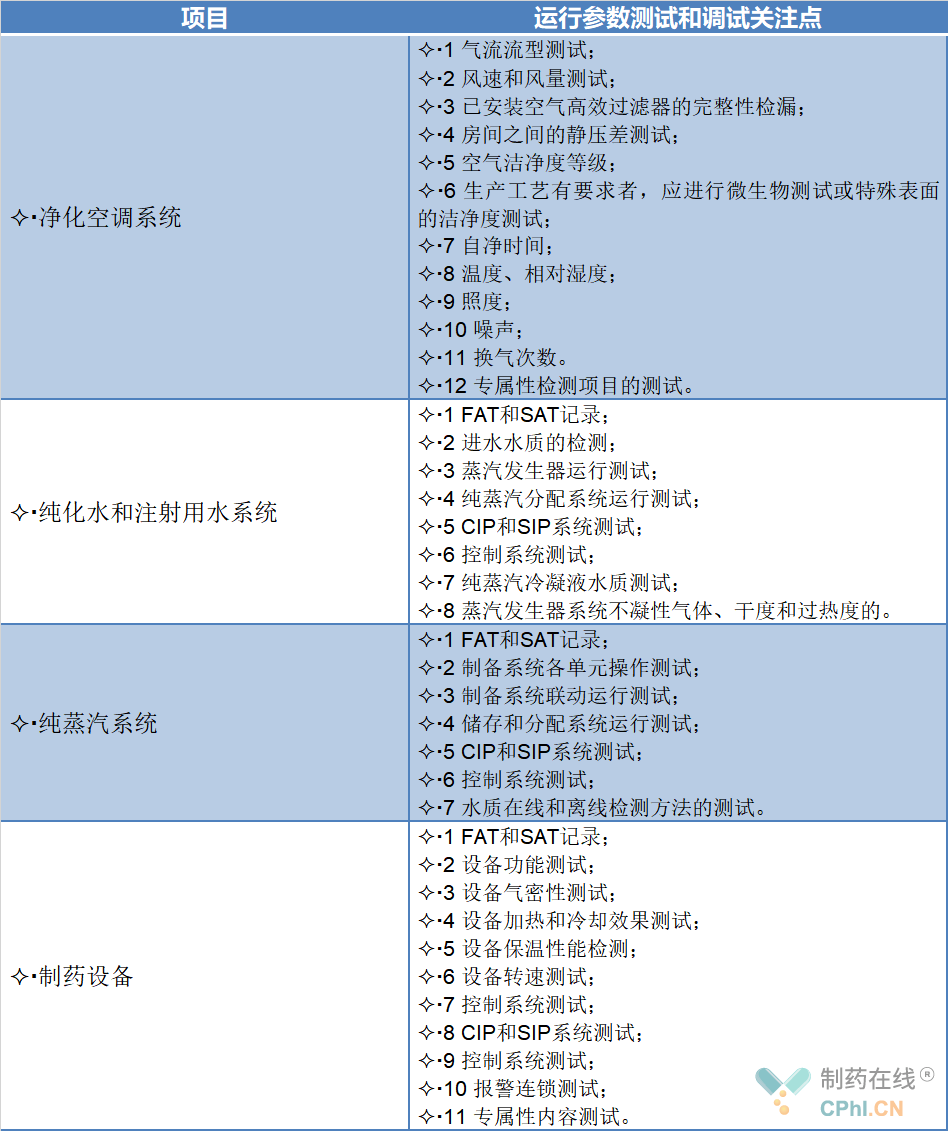
本标准明确提出,医药工业洁净厂房的施工验收,应在各单元单机测试,无生产负荷系统测试合格后进行。除常规施工验收内容外,医药洁净区机械施工验收包括净化空调系统运行参数测试和调试、纯化水和注射用水系统测试和调试、纯蒸汽系统测试和调试、制药设备测试和调试,以及医药洁净区内各单元观感质量核查,医药洁净区内各单元观感质量核查应符合本标准的相关规定,房施工验收后,应由施工方编写施工验收文档,该文档应作为运行确认和性能确认依据之一,具体内容详见下表:
参考文献
[1]www.mohurd.gov.cn
作者简介:滴水司南,男,生物医药高级工程师,立足于生物医药行业质量管理工作,专注于生物医药产业。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57