2019年07月05日,海南省药品监督管理局官网发布了《药品生产企业部分关键人员年度考试办法》征求意见稿,会稿截止日期2019年07月14日,弥补了国内对药品生产企业关键人员考核管理法规层面上的空白,对促进药品生产企业关键人员加强药品监管法律法规和药品生产、质量管理业务知识学习,提升管理能力具有深远的意义,本文对药品生产企业部分关键人员考核管理的痛点、难点和关键点进行了分析。
一、药品生产企业关键人员管理痛点
药品生产企业关键人员是指:企业负责人、生产管理负责人、质量管理负责人和质量受权人。随着国家药监部门逐渐加大对市场上药品的监管力度,越来越多的药品生产企业暴露出关键人员管理上的问题,比如2018年长春长生**事件,暴露出该企业管理人员GMP意识不健全,企业关键管理人员直接参与实施违法行为。特别是近期曝光的某省部分中药饮片小微生产企业,企业法人缺乏相关法律意识、责任意识和质量意识,急需制定出药品生产企业关键人员的专业知识和法律教育相关制度。
二、药品生产企业关键人员管理难点
药品生产企业关键人员资质、职责界定和培训管理上存在较多问题,笔者梳理了近几年药品飞行检查通告中常见的人员关键人员管理方面的缺陷,希望对药品生产企业有所参考,加强企业自身的检查并严格按照要求进行管理,主要缺陷有:
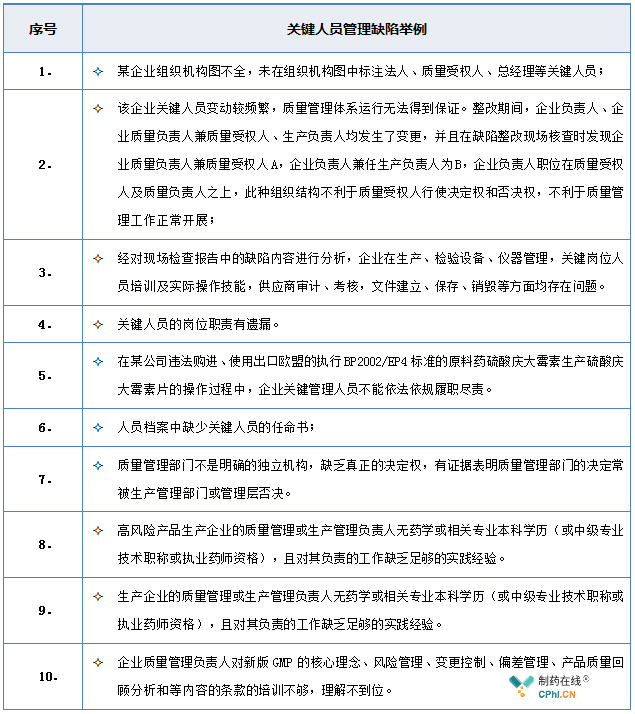
三、药品生产企业关键人员管理关键点
为促进药品生产企业落实药品生产质量管理主体责任,更好地发挥关键岗位人员在企业药品质量管理体系中的关键作用,近日,海南省药监局发布的《药品生产企业部分关键人员年度考试办法》(征求意见稿),对药品生产企业部分关键人员考核内容、考核程序、结果处理等方面作了明确规定要求,实行分级分类管理,通过加强关键人员考核和评价,将对关键岗位人员有效履职发挥重要作用,切实提高企业药品质量管理水平,只有把药企部分关键人员的法律意识、责任意识和质量意识提高,才能在药品质量安全的环节有更好的保障,海南省药监局发布的《药品生产企业部分关键人员年度考试办法》对关键人员管理的提出了更具有可操作性的办法。
3.1 引入第三方专业机构做评价,年度考核将更具可操作性
海南省药品监督管理局药品注册与生产监管处负责每年对药品生产企业关键人员考试一次。上半年通知考试范围,下半年安排考试,期间不组织、安排培训,不推荐参考书籍,由企业人员自学。药品注册与生产监管处委托第三方专业考试机构出题、制作准考证、组织笔试、阅卷、统计分数、反馈成绩等。
3.2 一场闭卷笔试 提升管理水平
根据管理岗位的类型,考试内容又再分为生产管理岗位和质量管理岗位,不同岗位人员考试相应的内容。企业负责人只参加基础部分考试。
考试方式为闭卷笔试。试卷内容分为基础部分和专项部分。
基础部分占50%,主要为药品管理法律法规规章、GMP常识等。
专项部分占50%,根据药品生产企业的类型,分为注射剂、口服制剂、原料药、中药饮片和医用氧五个不同专业版块知识。参加考试人员根据所在企业的生产范围,考试相应的专项部分知识。所在企业有以上多个生产范围的,以所在企业常年生产且产量大、市场占有率高的品种确定考试专项部分。
3.3 分级分类管理 成绩将排名
根据各专项考试的人数确定参考人员考试成绩的等次,各专项考试前三分之一的为A级,中间三分之一的为B级,后三分之一的为C级。药品注册与生产监管处将各专项考试排名为A的在全行业公布,排名为B的向企业和参考人员反馈成绩,排名为C 的只向参考人员本人反馈成绩。企业负责人的成绩不排名,只向本人反馈。
3.4 落实负面清单
对有下列情形的企业,将约谈企业负责人,要求加强对关键人员的培训教育,并下调一级下一年度分级分类管理档次:
(一)有参考人员连续两年排名最后三名的;
(二)缺考人员达到2名及2名以上的(缺考不再组织补考);
(三)考试中有夹带、抄袭、替考、将通讯工具带入考场等舞弊行为的。
参考文献:
[1] hifda.hainan.gov.cn/hifda/xxgk/tzgg/201907/t20190705_2625038.html
[2] www.sohu.com/a/237331809_100006541
作者简介:滴水司南,男,生物医药高级工程师,立足于生物医药行业质量管理工作,专注于生物医药产业,希望在知识的海洋里,用简单的语言讲述不简单的专业知识,提供一枚知识的指南针,指引读者到达知识的彼岸。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57