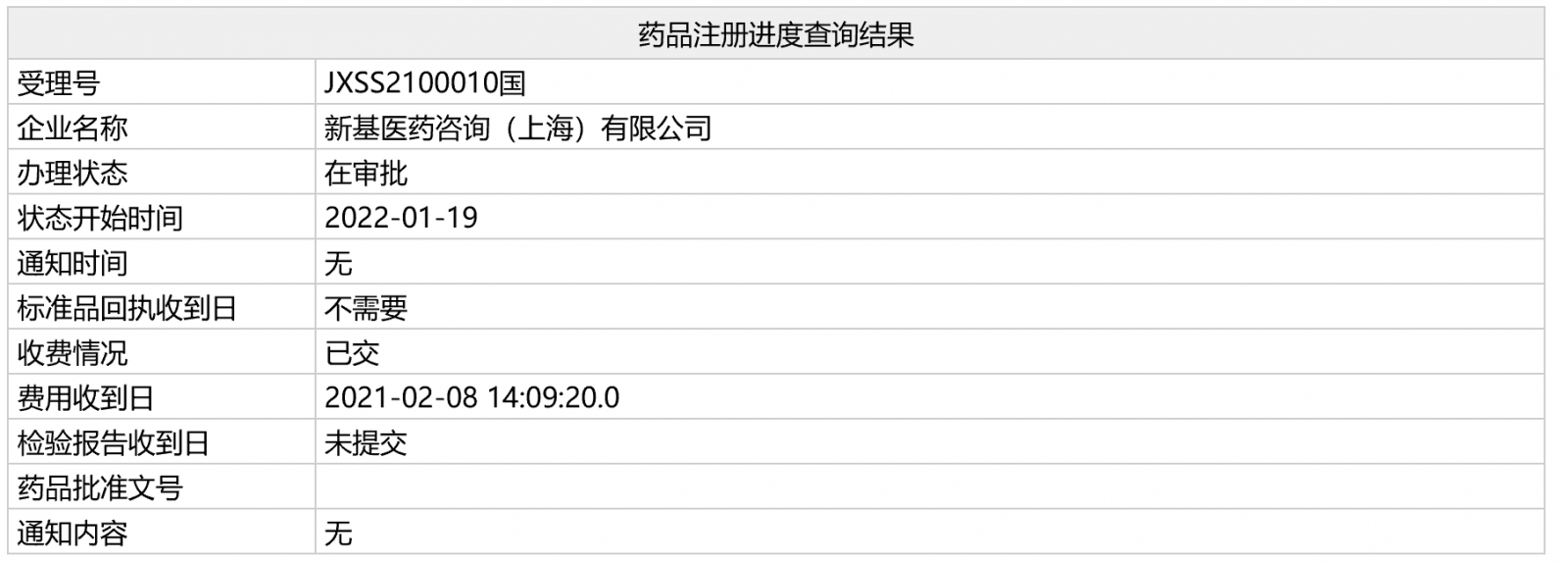
日前,新基「注射用罗特西普」的上市申请(相关受理号为JXSS2100010、11)在NMPA的状态变更为“在审批”,预计不日将正式获批,用于治疗需要定期输注红细胞(RBC)的成人β-地中海贫血患者。
罗特西普(Luspatercept,Reblozyl)是一种首创的红细胞成熟剂,可调节晚期红细胞的成熟。该药是一种可溶性融合蛋白,由人IgG1的Fc结构域与激活素IIB型受体(ActRIIB)胞外结构域融合而成,作为一种配体陷阱,通过靶向结合可调节晚期红细胞(RBC)成熟的转化生长因子(TGF)-β超家族的特定配体,减少Smad2/3信号通路的激活,改善无效红细胞的生成,促进晚期红细胞的成熟,提高血红蛋白水平。
目前,Reblozyl在美国获批2个适应症:(1)需要定期输注红细胞的β地中海贫血成人患者的贫血(2019.11);(2)低危骨髓增生异常综合症(MDS)成人患者相关的贫血(2020.04)。此外,Reblozyl用于非输血依赖型(NTD)β地中海贫血成人患者相关贫血的sBLA正在美国接受审查,PDUFA日期为2022年3月27日。
Reblozyl最初由BMS与Acceleron制药公司(后被默沙东以115亿美元收购)合作开发,是首 个获得监管批准用于治疗β-地中海贫血、极低/低/中危骨髓增生异常综合征(MSD)相关贫血的红细胞成熟剂(EMA),业界预测其未来年销售额有望突破20亿美元。据悉,Reblozyl 2020年销售额为2.74 亿美元,2021上半年销售额达2.4亿美元。
在国内,罗特西普用于需要定期输注红细胞(RBC)成人β-地中海贫血患者的新药申请于2021年2月获CDE受理,据悉该上市申请是基于国外临床试验BELIEVE 的数据。该研究是一项随机、双盲、安慰剂对照、多中心3期临床研究,共入组336名患者,在全球15个国家65个临床试验中心开展,旨在比较 Luspatercept+最 佳支持治疗(BSC)与安慰剂+BSC 对需要定期输注红细胞的成人β地中海贫血患者的疗效。
结果显示,经Luspatercept治疗后,21.4%患者的输血负担与基线相比降低超过 33%,显著优于安慰剂组(4.5%)。而且,Luspatercept还能显著降低输血依赖型β-地中海贫血患者血清铁蛋白水平。
β-地中海贫血是由于β-珠蛋白基因异常而导致的单基因遗传病,是地中海贫血中最常见的类型,据悉我国整体人群的患病率为 0.67%。目前,β-地中海贫血的治疗方法包括输血、铁螯合、脾切除、造血干细胞移植等,其中造血干细胞移植是目前唯一可治愈β-地中海贫血的手段,但配型成功概率低,价格高昂,且患者年龄越小效果越好,通常在8岁以下儿童中进行。罗特西普作为一种首创的红细胞成熟剂,有望为β-地中海贫血患者带来新选择。
此外,目前国内还有一款在研β-地中海贫血新药,即博雅辑因的ET-01。ET-01是一款处于研发阶段的、自体的、体外基因编辑细胞疗法产品,其原液通过采集患者自体动员外周血单个核细胞,富集CD34+细胞群后用CRISPR/Cas9系统编辑BCL11A基因的红系增强子制成。2021年1月,ET-01在国内获批临床,适应症为:不能接受常规干细胞移植的输血依赖型β地中海贫血。值得一提的是,ET-01是我国首 个获批开展临床试验的基因编辑疗法和造血干细胞疗法研究产品。



合作咨询
![]() 肖女士
肖女士
![]() 021-33392297
021-33392297
![]() Kelly.Xiao@imsinoexpo.com
Kelly.Xiao@imsinoexpo.com
 2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57
2006-2025 上海博华国际展览有限公司版权所有(保留一切权利)
沪ICP备05034851号-57